監修
東京都健康長寿医療センター 脳神経内科 医長
井原 涼子 氏
本邦における認知症の患者数は2025年に約472万人、2060年には約645万人に達すると推測されており、患者さんやその家族のみならず、社会全体に対する影響は深刻さを増しています。そうした中、認知症治療は大きな転換期を迎え、従来の対症療法に加えてアルツハイマー病の病態に働きかける疾患修飾薬が登場しました。今回の特集では、認知症治療の最前線で活躍している東京都健康長寿医療センター脳神経内科医長の井原涼子氏に、認知症として最も多いアルツハイマー型認知症に対する薬物療法の現状と課題、今後の展望についてお話いただきました。
アルツハイマー型認知症の原因はアミロイドβの蓄積
認知症は、一度は正常に発達した認知機能が何らかの原因により徐々に低下し、日常生活に支障をきたす状態です。認知症の中で最も多いのがアルツハイマー型認知症で全体の約6割、次いで脳血管性認知症が約2割、レビー小体型認知症が約1割程度となっています。
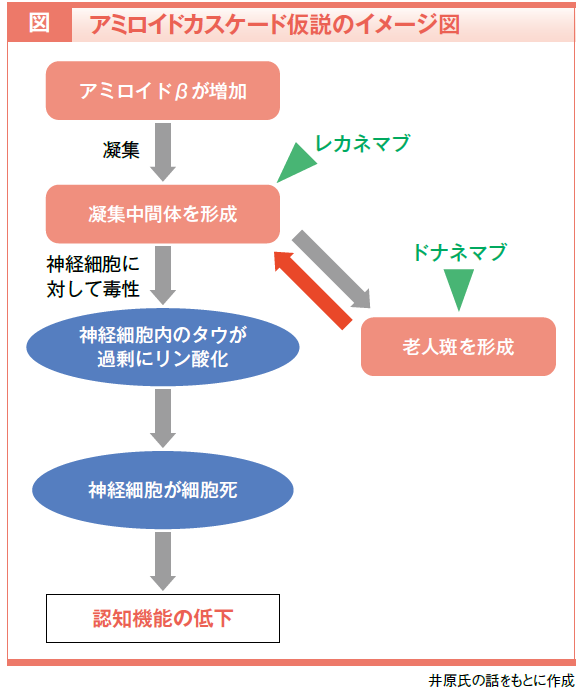
アルツハイマー型認知症の原因のひとつとされているのがアミロイドβの蓄積です。脳の神経細胞から分泌されるアミロイドβという蛋白質が何らかの原因によって過剰になると、徐々に凝集して凝集体を形成し、最終的に老人斑という塊になり細胞外に沈着します。凝集する過程で生じる凝集中間体は神経細胞に対して強い毒性を持っており、凝集中間体はシナプスに作用し、神経細胞内でタウという蛋白質の過剰なリン酸化が引き起こされ、最終的に細胞死に至ります。この流れはアミロイドカスケード仮説と呼ばれ、長い年月をかけて脳内に広がり、認知機能を徐々に低下させます(図)1)。
アルツハイマー型認知症の中心的な症状は記憶障害
アルツハイマー型認知症の症状は、脳が障害されたことによって現れる中核症状と、脳の障害を背景にして体調や心理状態、生活環境などの影響が加わって現れる行動・心理症状(Behavioral and Psychological Symptoms of Dementia: BPSD)に大別できます。
● 中核症状
中核症状は、記憶、注意、遂行機能、言語、視空間認知、行為といった認知領域に機能低下が生じたことで起こる症状です(表1)。アルツハイマー型認知症の典型例では、記憶障害が中心的な症状であり、最も早く出現します。新しいことを覚えられない、同じ物を何度も買ってくる、財布や鍵などの置き場所を忘れていつも探しているなどが頻繁に起こります。注意や視空間認知の低下も比較的早期から認められ、言語障害や行為などの低下は病気の進行に伴い現れます。
● BPSD(行動・心理症状)
BPSDを評価する指標として神経精神症状評価票があり、認知症で出現する12症状(妄想、幻覚、興奮、うつ、不安、多幸、無関心、脱抑制、易怒性、異常行動、夜間行動、食行動)が挙げられています2)。このうち、アルツハイマー型認知症では不安や不安に伴う焦燥感、うつ、意欲低下(無関心)、徘徊(異常行動)、妄想(物盗られ妄想など)などがよく見られます。不安や焦燥感は比較的早い時期でもよく見られ、中でも不安は、認知症に至る前の軽度認知障害(Mild Cognitive Impairment; MCI)の段階から出現していることがあります。興奮に伴う攻撃性や易怒性は、アルツハイマー型認知症の進行とともに現れるようになり、アルツハイマー型認知症が重度に至ると徘徊などが出てくることもあります。
BPSDの治療は、可能な限り非薬物療法、すなわち原因(薬剤、合併症、環境の変化など)の除去から始め、それが難しい場合には、それぞれの症状に応じた薬物療法を行います。
アルツハイマー型認知症の薬物療法
アルツハイマー型認知症に対する従来の薬物療法は、症状を一時的に軽減する対症療法でした。しかし、2023年および2024年に疾患修飾薬である抗アミロイドβ抗体薬(レカネマブ、ドナネマブ)が登場したことにより、治療の目的はアルツハイマー病の病態を改善し、進行を抑制することへとシフトしました。いずれの薬も、従来の薬物療法よりも早い時期、アルツハイマー病による軽度認知障害から軽度の認知症に対して適応となっています。
レカネマブ、ドナネマブにより認知機能の悪化が緩やかに
レカネマブ、ドナネマブはアミロイドカスケード仮説に基づいて作られた薬剤であり、両薬剤とも神経細胞の外に蓄積したアミロイドβを除去する作用があります1)。作用機序において両薬剤が異なっているのは、レカネマブが主に凝集中間体に作用するのに対し、ドナネマブは主に凝集度の高い老人斑に作用する点です。
脳内のアミロイドβを除去することにより、それ以上の病態の進行を抑制し、認知機能の悪化が抑制されることが臨床試験で示されています。レカネマブの第Ⅲ相試験では、治療開始から18ヵ月後にレカネマブ群でプラセボ群に比べて認知機能の悪化が27.1%抑制されました3)。ドナネマブの第Ⅲ相試験では、治療開始から76週後にドナネマブ群でプラセボ群に比べ認知機能の悪化が28.9%抑制されました4)。
抗アミロイドβ抗体薬は、認知症の進行を止めたり、症状を改善したりするのではなく、進行のスピードを緩める治療であるため、治療効果がわかりにくいのが難点です。患者さんに説明する時は「レカネマブまたはドナネマブの治療をすると、治療を始めた時の認知症のレベルから重度になるまでの期間が、治療をしない時に比べて約1.4倍延びます」と説明しています。アルツハイマー型認知症が進行すると介護が必要になりますが、治療によって介護の必要がない期間が1.4倍に延長するのであれば、患者さんや家族にとって価値のあることだと思います。
主な副作用は脳浮腫、脳微小出血
抗アミロイドβ抗体薬の重要な副作用は、MRI検査で認める脳浮腫や脳微小出血などです。これらを「アミロイド関連画像異常(Amyloid-Related Imaging Abnormalities; ARIA)」と呼びます。ARIAにより意識障害や痙攣など重篤な事象が起こる恐れがあるので早期に発見することが大切です。臨床試験データにおけるARIAの発現頻度は、レカネマブで脳浮腫が12.6%、脳微小出血などが13.6%3)、ドナネマブでそれぞれ24.0%、31.4%などでした4)。一方、このうち症状を伴うものは一部にとどまりますので、ARIAの有無を確認するため、治療中はMRI検査を定期的に行うことになっています。この他に、インフュージョンリアクションもよくみられる副作用です(表2)。
レカネマブ、ドナネマブ治療を受けられる患者
抗アミロイドβ抗体薬が世に出てから、当院で抗アミロイドβ抗体薬の治療を希望し、検査を受けた患者さんのうち、実際に治療を実施できた割合はわずか20%にとどまります。抗アミロイドβ抗体薬による治療を受けられるのは、アルツハイマー病による軽度認知障害および軽度の認知症で、MMSEやCDRといった検査では評価の範囲が限られています。そしてアミロイドPETや脳脊髄液検査でアミロイドβの蓄積が認められた患者さんに限られます。たとえアミロイドβの蓄積があっても、症状がない、あるいは中等度以上のアルツハイマー型認知症の場合、治療の対象にはなりません。また、MRI検査を受けられることが条件で、治療前の検査で脳浮腫や脳微小出血などが見つかった患者さんには禁忌となります。
抗アミロイドβ抗体薬治療の課題
レカネマブは2週に1回、ドナネマブは4週に1回、いずれも静脈点滴で投与します。レカネマブの治療期間は原則として18ヵ月間で、18ヵ月後の効果をみて、治療を続けるか中止するかを判断します。一方、ドナネマブの治療期間は最長で18ヵ月間と決まっています。治療期間中は定期的にMRI検査や認知機能検査を行う必要があり、これには家族や介護者の協力が欠かせません。このため、治療を継続するには協力してくれる家族や介護者の存在は大きな鍵になります。
高齢の患者さんや付き添う家族にとって、通院の負担が大きいことは言うまでもありません。また、抗アミロイドβ抗体薬の治療には高額な費用がかかり、自己負担の割合などによっても異なりますが、月1.8~10万円程度が必要なため、経済的な負担で治療の選択を悩まれる患者さんもいます。
抗アミロイドβ抗体薬の治療が受けられるかどうかを知るためには、数種類の認知機能検査、MRI検査、アミロイドPETまたは脳脊髄液検査を受ける必要がありますが、これらの検査を実施できる医療施設は限られています。また、抗アミロイドβ抗体薬を投与開始できる医療施設には、認知症診療の経験が10年以上ある専門医が複数名いること、MRI検査ができること、副作用に対応できる体制があることなど厳しい条件があり、地域によっては通院できる範囲に投与可能な施設がないこともあります。さらに、投与可能な施設でも点滴ブースの不足という問題が生じており、治療アクセスを改善することが今後の課題といえるでしょう(表3)。
症状の改善を目指す薬物療法
認知症のさまざまな症状を改善するため、コリンエステラーゼ阻害薬やNMDA受容体拮抗薬が従来から使用されています。これら2剤は併用されることもあります。
● コリンエステラーゼ阻害薬
アルツハイマー型認知症では、脳神経細胞の障害が広がるに伴ってアセチルコリン(記憶や学習に関わる神経伝達物質)が減少するため、記憶や学習の機能が低下します。コリンエステラーゼ阻害薬はアセチルコリンを分解する酵素の働きを抑制することで脳内のアセチルコリン濃度を上昇させ、神経伝達を促進します。
コリンエステラーゼ阻害薬にはドネペジル、リバスチグミン、ガランタミンがあります。ドネペジルは経口薬と貼付薬があり、ガランタミンは経口薬、リバスチグミンは貼付薬です。各薬剤の適応はアルツハイマー型認知症の重症度によって異なり、ドネペジルは軽度から重度まで使用可能ですが、他の2剤は軽度および中等度が対象となります。3剤とも主な副作用は嘔気などの消化器症状です。経口投与が可能であれば1日1回の服薬ですむドネペジルを使用することが多く、嘔気などを避けたい場合はドネペジルの貼付薬やリバスチグミンが選択肢となります。
● NMDA受容体拮抗薬
アルツハイマー型認知症では、神経細胞の変性により興奮性神経伝達物質であるグルタミン酸の細胞外濃度が高まり、グルタミン酸の受容体であるNMDA受容体が過剰に活性化されます。その結果、神経細胞内にカルシウムイオンが過剰に流入し、神経細胞傷害が引き起こされます。NMDA受容体拮抗薬であるメマンチンは、NMDA受容体の過活性を抑制することにより神経細胞を保護します。
メマンチンは中等度から重度のアルツハイマー型認知症が適応で、主な副作用はめまい、頭痛、便秘などです。メマンチンは興奮性の神経伝達を抑制するので、興奮性のBPSDを抑えるためによく用いられます(表4)。
BPSDに対する薬物療法
BPSDの各症状は、コリンエステラーゼ阻害薬やNMDA受容体拮抗薬により軽減することがありますが、それらで効果が足りない場合には非定型抗精神病薬などを使用します。
不安に対しては非定型抗精神病薬であるリスペリドンやオランザピン、クエチアピン、焦燥感に対してはリスペリドンやアリピプラゾール、ブレクスピプラゾールなどの使用を検討します。幻覚・妄想に対してはリスペリドンやオランザピン、クエチアピン、アリピプラゾールなど、徘徊に対してはリスペリドンの使用を検討します5)。この中で、ブレクスピプラゾールがアルツハイマー型認知症に伴うBPSDの一部の症状に対する適応承認を取得しています。ブレクスピプラゾールの効能・効果は「アルツハイマー型認知症に伴う焦燥感、易刺激性、興奮に起因する、過活動又は攻撃的言動」です。なお、リスペリドンはドパミン遮断作用があり、副作用としてパーキンソニズムが発現することがあるので、レビー小体型認知症を合併しているアルツハイマー型認知症患者さんには使用しにくいです。また、クエチアピンとオランザピンは副作用として高血糖をきたすことがあるので、糖尿病のある患者さんには禁忌です。
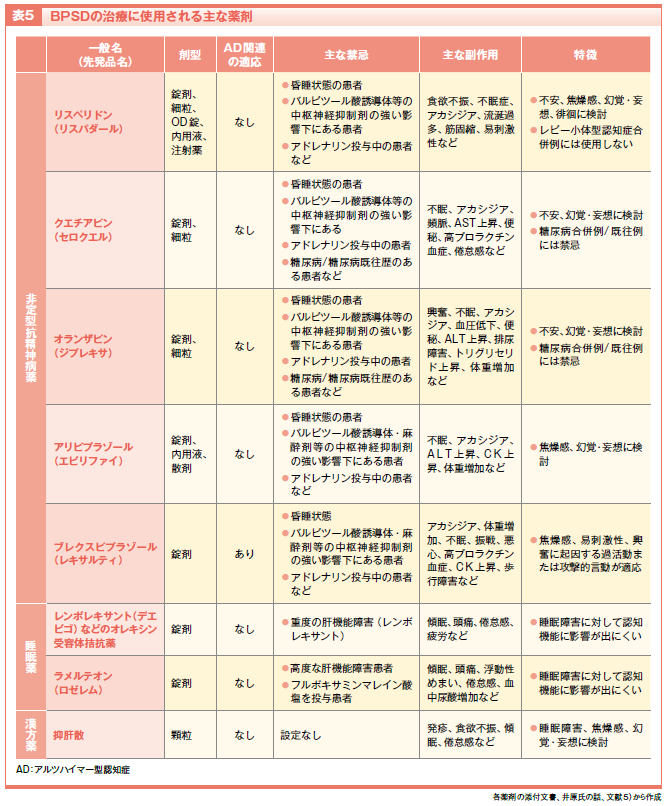
この他に、抑肝散を焦燥感、易怒性、幻覚・妄想に対して使用することがありますし、睡眠障害に対しては認知機能に影響が出にくいオレキシン受容体拮抗薬やラメルテオンを用います(表5)。
認知症治療で薬剤師に期待される役割
認知症の患者さんは複数の薬剤を併用していることが多いのですが、認知機能の低下が進むと薬剤管理が難しくなります。そのため、必要に応じて訪問薬剤師に入ってもらうなど安全に服薬できる環境を整えてから治療薬を処方するようにしています。今後、独居の高齢者が増えると予測されていることを考えると、訪問薬剤師の存在がより重要になるでしょう。
患者さんの認知機能の低下に最初に気付くことが多いのは薬剤師です。薬剤管理ができないことは認知機能が低下している、特に認知症の状態になりつつあるサインであり、かかりつけ薬局から「患者さんの認知機能を調べて欲しい」という連絡が来ることは珍しくありません。独居の高齢者は認知機能低下があっても気付かれにくいので、薬剤師が認知症のスクリーニング的な役割を担ってくれると早期発見の助けになると考えます。
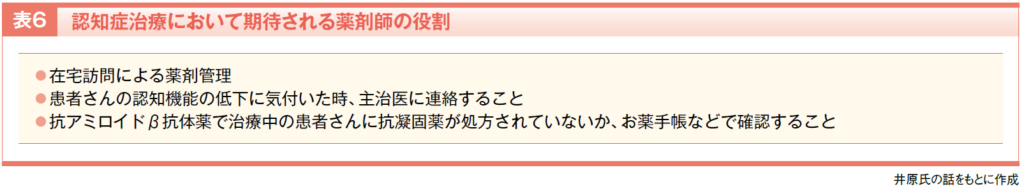
また、抗アミロイドβ抗体薬による治療を受けている患者さんでは、抗凝固薬の使用により副作用である脳出血の発現リスクが高まるため注意が必要です。レカネマブ、ドナネマブを使用している患者さんは治療カードを携帯したり、お薬手帳にその旨を示すシールが貼付されていたりするはずですので、それらに気付いたら、他の医療施設から抗凝固薬が処方されていないか確認してあげてください(表6)。
アルツハイマー病治療の今後の展望
アルツハイマー病による軽度認知障害から軽度認知症の進行を抑制する治療薬が登場したことは大きな進歩ですが、検査や治療を行える医療施設が限られているので、今後、これらの施設の拡充が望まれます。現在、抗アミロイドβ抗体薬の皮下注射薬の開発が進行中であり、臨床実装されれば治療を受けられる患者さんが増える可能性があります。
認知症の予防にも関心が高まっています。本邦における認知症患者数は今後も増加が見込まれていますが、増加のスピードは従来の予測よりも緩やかになっており6)、その背景には生活習慣の改善があると考えられています。認知症は、循環器系疾患や癌に続く「第三の生活習慣病」と呼ばれており、生活習慣の改善により認知機能の低下を予防できることがフィンランドのFINGER研究でも示されています7)。アミロイドβはアルツハイマー病の症状が出現する約15~20年前から蓄積し始め、早ければ40歳代から蓄積していることもあるため、早い時期に生活習慣を見直すことが重要です。薬物療法としては、現在、症状が発現する前に抗アミロイドβ抗体薬による予防的治療を開始する臨床試験が進行中です。
認知症はもはや糖尿病や高血圧と同じコモンディジーズであり、社会全体で患者さんと家族を支えていくことが必要です。その中で薬剤師には、薬剤管理のサポートや、日々出会う患者さんの認知機能低下をいち早く発見するスクリーナーとしての役割を期待します。
【参考文献】
1) 井原涼子. 薬局 2025; 76(1): 54-58.
2) 株式会社マイクロン. NPI 検査用紙.(2025年7月1日閲覧)
3) エーザイ株式会社/バイオジェン・ジャパン株式会社. レケンビ点滴静注添付文書. 2024年6月改訂(第3版)
4) 日本イーライリリー株式会社. ケサンラ点滴静注液添付文書. 2024年11月改訂(第2版)
5) 日本神経学会監. 認知症疾患診療ガイドライン2017. 医学書院, 2017年.
6) 内閣府. 令和6年版高齢社会白書(全体版). https://www8.cao.go.jp/kourei/whitepaper/w-2024/html/zenbun/index.html(2025年6月30日閲覧)
7) Ngandu T, et al. Lancet 2015; 385(9984): 2255-2263.
井原 涼子 氏
2002年東京大学医学部卒業。初期研修後2004年東京大学神経内科に入局。2011年東京大学大学院医学系研究科脳神経医学専攻修了、博士(医学)。2012年より東京大学医学部附属病院早期・開発探索推進室、ワシントン大学セントルイスKnight Alzheimer Disease Research Center等でアルツハイマー病の臨床研究に携わり、2020年より現職。抗アミロイドβ抗体薬の臨床実装を担っている。