監修
大阪国際がんセンター 呼吸器内科 副部長
國政 啓 氏
肺がんは死亡数の多いがんで、発見時にすでに進行期のケースもあります。その一方、特に非小細胞肺がんにおいては従来の抗がん剤のみならず、分子標的治療薬や免疫チェックポイント阻害薬など多くの薬剤が臨床に登場し、治療方針の決定にあたっては遺伝子変異などバイオマーカー検査の実施も必須となってきています。今回、大阪国際がんセンター 呼吸器内科副部長の國政啓氏に、非小細胞肺がんの進行期における薬物療法の動向を中心にご解説いただきました。
がんのなかで死亡数の多い肺がん
死亡数は男性で1位、女性で2位
「がんの統計」では、2023年のがん死亡は38万2,504人で、肺がんは男性でがん死亡の1位(52,908人)、女性では大腸がんに次いでがん死亡の2位(22,854 人)となっています1)。肺がんの危険因子のひとつは喫煙で、喫煙者が肺がんになるリスクは非喫煙者に比べ男性で4.4倍、女性で2.8倍ですが2)、非喫煙者が肺がんになることもあります。
肺がん検出の検査としては胸部X線検査が推奨されており、胸部X線検査で肺がんを疑う所見を認めた場合には胸部CT検査を行います。しかし、発見時にすでに進行期になっているケースも多く、肺がんによる死亡率の低下には胸部X線検査のみでは不十分です。肺がんは早期発見が重要であるものの、検診でのCT検査の実施については過剰診断の懸念や医療費などが課題となっています。
生検での検体採取と組織診断がほぼ必須
肺がんの確定診断においては、画像診断のみならず、病変部から採取した組織や細胞を用いた病理診断が必要です。病変が小さいⅠ期やⅡ期など、手術後でなければ組織の採取が困難な早期がんを除けば、ある程度の大きさの組織を採取して治療開始前に確定診断を行います。検体を採取する生検には気管支鏡検査のほかCTガイド下や超音波ガイド下の生検もあり、生検が困難な場合には胸水から採取した細胞による細胞診を実施します。
肺がんは非小細胞肺がんと小細胞肺がんに大別され、それぞれの治療方針は大きく異なります。近年、非小細胞肺がんに対してはがん発生の直接的な原因となるようなドライバー遺伝子変異を標的とした多くの分子標的治療薬が使用可能で、治療方針の決定においてはドライバー遺伝子変異の検査が必須とされています。
薬物療法の中心は進行期
近年は早期や周術期にも検討
非小細胞肺がんの薬物療法の対象はこれまで進行期(Ⅳ期)が中心でしたが、現在はⅢ期で放射線療法と薬物療法を併用する化学放射線療法や、Ⅱ期での術後の根治率を高めるために術前に薬物療法を行うこともあり、薬物療法の範囲は拡大しています。
薬物療法の実施に際しては個々の患者の状態を総合的に判断し、高齢でも全身状態が良好であれば、近年登場した免疫チェックポイント阻害薬の使用なども含め、積極的な治療を考慮するケースもあります。
Ⅳ期の非小細胞肺がんでは
9つの遺伝子変異を検査する
進行期(Ⅳ期)の非小細胞肺がんに対する薬物療法では、治療方針を決定するため9つのドライバー遺伝子変異(EGFR、ALK、ROS1、BRAF、MET、RET、NTRK、KRAS、HER2)を検査します(表1)。複数の遺伝子を同時に検査するマルチコンパニオン診断薬(CDx)として、次世代シークエンス解析(NGS)法によるオンコマインDxTT、肺がんコンパクトパネル、MINtS、リアルタイムPCR法を用いたAmoyDxの4つが保険収載されています(2025年12月時点)3)。
ドライバー遺伝子変異のなかで最も多いのはEGFR遺伝子変異で、その他の変異は低頻度です。日本において非小細胞肺がんのうち腺癌では、EGFR遺伝子変異53.0%、ALK 融合遺伝子変異3. 8%、MET融合遺伝子(エクソン14スキッピング)変異2.8%、HER2遺伝子変異1.9%、RET融合遺伝子変異1. 9%、ROS1融合遺伝子変異0. 9%、BRAF遺伝子変異0. 3%との報告もあります4)。
9つのうち6つのドライバー遺伝子変異(EGFR、ALK、ROS1、BRAF、MET、RET)については、遺伝子変異に対応した分子標的治療薬が一次治療から使用可能です。なお、ドライバー遺伝子変異が陰性だった場合にはPD-L1検査を行い、免疫チェックポイント阻害薬の使用を考慮します(表1)。
EGFR遺伝子変異陽性例では
変異に応じた治療を選択
9つのドライバー遺伝子変異で頻度の高いEGFR遺伝子変異としては、エクソン19欠失またはエクソン21のL858R変異が約90%を占めます。このほか、エクソン18-21にわたる遺伝子変異の頻度は低いためにuncommon mutationといわれます。
EGFR遺伝子変異に対する一次治療では遺伝子変異別に、上皮成長因子受容体チロシンキナーゼ阻害剤(EGFR-TKI)、二重特異性抗体(アミバンタマブ)、血管新生阻害薬、抗がん剤(プラチナ製剤、ペメトレキセド)による治療レジメンが肺癌診療ガイドライン2025(Web版)に記載されています(表2、表3)。
2025年の診療ガイドラインの改訂では、ラゼルチニブ+アミバンタマブ併用療法とオシメルチニブ+プラチナ製剤+ペメトレキセド併用療法が一次治療の選択肢として追加されました。これらのレジメンはEGFR-TKI単剤療法に比べ生存期間の延長を認めている一方で副作用に関する懸念もあり、全身状態が良好な患者において考慮します。なお、現在使用可能な治療レジメンからどのレジメンを選択するかは臨床的な課題となっています。
● EGFR-TKI
EGFR遺伝子変異陽性例に対するEGFR-TKIには、第一世代のゲフィチニブ、エルロチニブ、第二世代のアファチニブ、第三世代のオシメルチニブ、ラゼルチニブがあります。EGFR-TKIでは皮疹、爪囲炎、下痢などの発現が多く、また重篤な副作用として間質性肺疾患(Interstitial Lung Disease:ILD)に注意が必要です。
● 二重特異性抗体
二重特異性抗体アミバンタマブはEGFRとMETの両方を阻害するため、皮疹が強く発現することがあります。ラゼルチニブ+アミバンタマブ併用療法特有の有害事象として、インフュージョンリアクション、末梢性浮腫などが認められています。また、深部静脈血栓症および肺塞栓症を含む静脈血栓塞栓症に注意が必要です。
● 血管新生阻害薬
抗VEGF抗体のベバシズマブはエルロチニブとの併用でGrade3以上の高血圧、蛋白尿、出血性事象などが認められています。抗VEGFR抗体のラムシルマブはエルロチニブとの併用でGrade3以上の高血圧や下痢、ざ瘡様皮疹が認められています。
ALK、ROS1、BRAF、MET、RETの変異には
分子標的治療薬による一次治療
EGFR遺伝子変異以外の頻度の低いドライバー遺伝子変異のうち、ALK、ROS1、BRAF、MET、RETについては、一次治療においてドライバー遺伝子変異に対する分子標的治療薬が使用可能です。患者数が少ないため薬剤同士を比較する第Ⅲ相試験の実施が困難で、主に単群の第Ⅱ相試験にもとづいて承認されています。実臨床においては、第Ⅱ相試験での有効性や特徴的な副作用、錠剤の大きさや服薬回数なども考慮して治療を決定します。
● ALK融合遺伝子陽性
ALK融合遺伝子陽性例では、一次治療のALK-TKIとしてPS0~1ではアレクチニブ単剤、ロルラチニブ単剤が強く推奨されており、PS2~4ではアレクチニブ単剤が強く推奨されています。アレクチニブ単剤療法では味覚障害、筋肉痛、皮疹のほか、間質性肺炎の発現に注意が必要です。ロルラチニブ単剤療法では特徴的な有害事象として認知機能障害があります。
● ROS1融合遺伝子陽性
ROS1融合遺伝子陽性例では、一次治療としてROS1-TKI単剤療法が強く推奨されており、クリゾチニブ、エヌトレクチニブ、レポトレクチニブ、タレトレクチニブが選択肢となっています。クリゾチニブでは視覚障害、消化器毒性、肝機能障害、エヌトレクチニブでは消化器毒性、倦怠感、浮腫、レポトレクチニブでは消化器毒性、めまいや運動失調、タレトレクチニブでは血液毒性や消化器毒性、めまいなどが認められています。
● BRAF遺伝子V600E変異陽性
BRAF遺伝子V600E変異陽性例では、一次治療としてBRAF阻害薬ダブラフェニブとMEK阻害薬トラメチニブの併用療法が強く推奨されています。発熱、肝機能障害、心駆出率減少などが認められています。
● MET遺伝子変異陽性
MET遺伝子変異陽性例では、一次治療としてMET-TKI単剤療法が強く推奨されており、テポチニブ、カプマチニブ、グマロンチニブのいずれかが強く推奨されています。テポチニブ、カプマチニブでは末梢浮腫、グマロンチニブでは浮腫などが認められています。
● RET融合遺伝子陽性
RET融合遺伝子陽性例では、一次治療としてセルペルカチニブ単剤療法が強く推奨されています。肝機能障害、高血圧、下痢、浮腫、皮疹などが認められています。
NTRK、KRAS、HER2変異は
二次治療以降で分子標的治療薬
NTRK融合遺伝子陽性例、KRAS遺伝子G12C変異陽性例、HER2遺伝子変異陽性例では、ドライバー遺伝子変異/転座陰性例の初回治療に準じて一次治療を行い、二次治療以降で分子標的治療薬が推奨されています。
● NTRK融合遺伝子陽性
NTRK融合遺伝子陽性例の二次治療以降では、TRK-TKI単剤療法としてエヌトレクチニブ、ラロトレクチニブのいずれかが強く推奨されています。エヌトレクチニブでは消化器毒性や浮腫など、ラロトレクチニブでは消化器毒性やめまいなどが認められています。
● KRAS遺伝子G12C変異陽性
KRAS遺伝子変異のなかのG12C変異陽性例に対しては、二次治療以降でソトラシブ単剤療法が強く推奨されています。ソトラシブ単剤療法では、下痢、悪心、倦怠感、肝機能障害などが認められています。
● HER2遺伝子変異陽性
HER2遺伝子変異陽性例では、二次治療以降において抗体薬物複合体のトラスツズマブデルクステカンや分子標的治療薬のゾンゲルチニブ単剤療法が強く推奨されています。トラスツズマブデルクステカンでは消化器毒性、血液毒性、間質性肺炎など、ゾンゲルチニブ単剤療法では消化器毒性、皮膚毒性などが認められています。
皮疹、浮腫や中枢神経症状などにも留意する
多くの分子標的治療薬のなかで特徴的な有害事象として、EGFR-TKIでは皮疹が発現しやすく、ALK-TKIのロルラチニブとTRK-TKIのレポトレクチニブは脳への移行性を高めるために薬剤に環状構造があるため、めまいやふらつきなどの中枢神経症状が発現します。また、MET阻害薬では末梢浮腫としての足のむくみが特徴的であり、EGFRとMETを阻害する二重特異性抗体のアミバンタマブでも浮腫が発現します。
PD-L1の発現を評価し
免疫チェックポイント阻害薬を検討
非小細胞肺がんに対する免疫チェックポイント阻害薬の使用にあたっては、採取した組織検体を用い、免疫組織化学染色(IHC)法により全腫瘍細胞に対してPD-L1陽性細胞が占める割合を示すTPS(Tumor Proportion Score)を評価します。PD-L1発現は、TPS 50%以上(陽性、高発現)、1~49%(陽性、低発現)、1%未満(陰性)に分けられます(表1)。
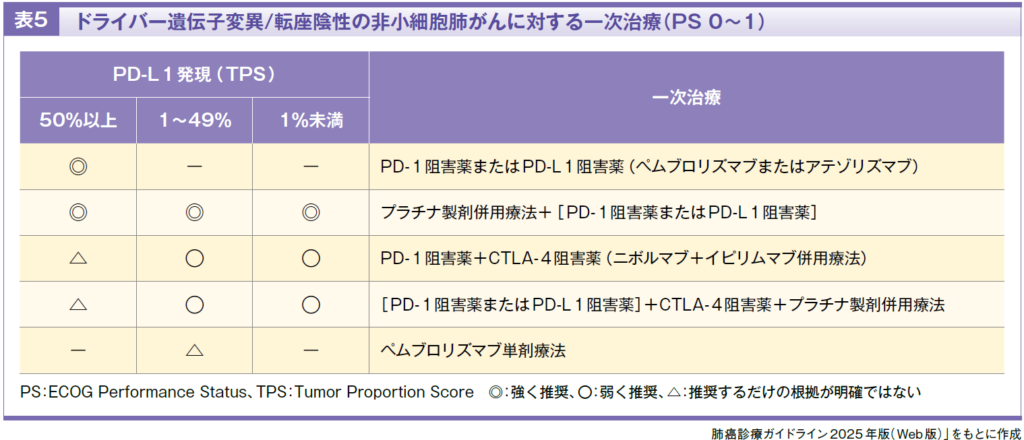
免疫チェックポイント阻害薬には、PD-1阻害薬のニボルマブ、ペムブロリズマブ、セミプリマブ、PD-L1阻害薬のアテゾリズマブ、デュルバルマブ、CTLA-4阻害薬のイピリムマブ、トレメリムマブがあり(表4)、治療の選択肢には、PD-1またはPD-L1阻害薬単剤、PD-1またはPD-L1阻害薬単剤とプラチナ製剤併用療法の併用、PD-L1阻害薬とCTLA-4阻害薬の併用療法、PD-L1阻害薬とCTLA-4阻害薬の併用療法にプラチナ製剤併用療法を併用、の4つがあります(表5)。
治療の選択においては、PD-L1発現(TPS)、患者の全身状態、副作用などを考慮します。TPSが50%以上の場合にはペムブロリズマブやアテゾリズマブの単剤治療による効果が期待され、PD-L1発現が50%未満の場合はこれらにプラチナ製剤併用療法を併用します。なお、PD-L1阻害薬とCTLA-4阻害薬の併用療法は副作用が強いため、その他の選択肢が考慮できる場合は積極的には選択されません。
臓器横断的な免疫関連有害事象にはチームで対応
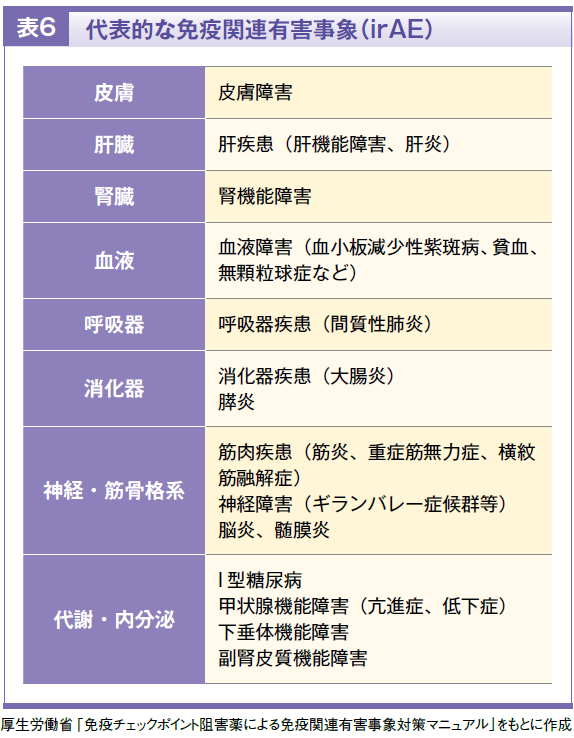
免疫チェックポイント阻害薬は免疫応答に抑制をかけるT細胞上の免疫チェックポイント分子を阻害してT細胞を再活性化しますが、T細胞の活性化により免疫関連有害事象(immune-related adverse events:irAE)が臓器横断的に発生します。irAEには、I型糖尿病や重症筋無力症など、これまでの抗がん剤や分子標的治療薬では経験しなかったような事象もあり(表6)、どのような患者でirAEが発現するかの予測も困難です。
そのため、発現する可能性のあるirAEについてはハンドブックなども用いて患者に説明し、irAEを疑う事象が発現した際に診療科横断的に相談が可能な窓口を院内に設置しています。免疫チェックポイント阻害薬は肺がん以外のがん腫でも使用され、多くの診療科の医師にとってirAEは懸念事項であることから、各医療機関においてはirAE対策チームなどを作って対応していると考えられます。
irAEの対応ではステロイド、
免疫抑制剤や生物学的製剤も使用
irAEの対応においては免疫を抑制する治療が中心となり、ステロイドや免疫抑制剤、抗IL-6抗体や抗TNF-α抗体などの生物学的製剤も使用されます。これらの薬剤はこれまでリウマチの専門医などが中心的に使用していた薬剤でもあり、がん専門施設では使用に精通している医師が少なく、薬剤師からの専門的なサポートも不可欠です。
薬剤師さんからは、ステロイド使用時には副作用を鑑み、胃潰瘍を予防するプロトンポンプ阻害薬が処方されているか、骨の脆弱化を抑制する薬が処方されているか、真菌感染を予防する抗菌薬(バクタ®など)が適切に処方されているかなどを確認していただくことも大切です。また、肝機能が悪い場合には抗TNF-α抗体の使用を控える必要があるため、肝機能を確認するなど、医師が見落としがちな点について薬剤師さんから注意喚起していただくことも重要です。
多くの新薬を届けるには
医療従事者の連携が必要
肺がん診療においては、過去の基礎研究の恩恵から多くの新薬が臨床に登場し、診療ガイドラインも年々改訂されています。一方で、高齢者や合併症のある患者を含め、新薬を適切に患者に届けるためには現場の医療従事者の協力が欠かせません。
医師が薬を処方していても、限られた診療時間では副作用の説明や服薬状況の確認などが十分にできているとは言い難く、またがん治療では内服薬も非常に高額ですが、服薬していると患者が述べていても、認知症などにより服薬されていないこともあります。
投与量の確認、副作用に関する説明、服薬状況の確認、処方されている薬剤の相互作用の確認など、薬剤師さんの専門的かつ医師とは異なる視点からのサポートや医師へのフィードバックは不可欠であり、複雑化するがん薬物療法において、医師、看護師、薬剤師などの職種が一体となって治療を成立させていくことが重要と考えています。
本記事のポイント
・がん死亡のなかで、肺がんは男性で1位、女性で2位
・胸部X線検査で肺がんを疑ったら胸部CT検査を行う
・組織型(非小細胞肺がん、小細胞肺がん)により治療方針が異なる
・Ⅳ期の非小細胞肺がんでは治療方針の決定にあたりバイオマーカー(ドライバー遺伝子変異やPD-L1発現など)の検査が必須であり、気管支鏡検査などにより組織検体を採取する
・6つの遺伝子変異については一次治療で遺伝子変異に基づいた治療、3つの遺伝子変異については二次治療で遺伝子変異に基づいた治療を行う
・PD-L1発現にもとづき、免疫チェックポイント阻害薬の使用を考慮する。irAEの発現と対処に留意する
【参考文献】
1)がんの統計編集委員会編.がんの統計〈2025年版〉.
https://www.fpcr.or.jp/pamphlet.html#cat7
https://www.fpcr.or.jp/pdf/pamphlet/cancer_statistics_2025.pdf#toolbar=0&navpanes=0′
2)Wakai K, et al. Jpn J Clin Oncol. 2006; 36: 309-24.
3)日本肺癌学会バイオマーカー委員会編.肺癌患者におけるバイオマーカー検査の手引き(2026年1月改訂v2.1.7)
https://www.haigan.gr.jp/publication/guidance/inspection/
4)Saito M, et al. Cancer Sci. 2016; 107 :713-20.
5)日本肺癌学会編.肺癌診療ガイドライン(胸膜中皮腫・胸腺腫瘍含む)2025年(Web版)
https://www.haigan.gr.jp/publication/guideline/examination/2025/
6)厚生労働省「免疫チェックポイント阻害薬による免疫関連有害事象対策マニュアル」
https://www.mhlw.go.jp/topics/2006/11/tp1122-.1q.html
https://www.mhlw.go.jp/topics/2006/11/dl/tp1122-1q05.pdf
國政 啓 氏
2006年大阪大学医学部医学科卒業、市立池田病院での初期臨床研修を経て、倉敷中央病院呼吸器内科で後期臨床研修を修了。2016年神戸大学大学院医学系研究科博士課程を修了(医学博士)。2017年より大阪国際がんセンター呼吸器内科に勤務。2022年より同副部長。日本肺癌学会ガイドライン、バイオマーカー委員。JCOG肺がん内科グループ代表委員。