監修
山梨大学大学院整形外科学講座 講師
大場 哲郎 氏
一般的に腰痛は高齢者に多いというイメージがありますが、腰椎椎間板ヘルニアは20~40歳代の働き盛りに多く発生し、高齢者での発症は少ない疾患です。激しい痛みを伴う腰椎椎間板ヘルニアはどのように発生するのか。病態から治療まで山梨大学大学院整形外科学講座 講師の大場哲郎氏に解説していただきました。
腰椎椎間板ヘルニアの病態
「ヘルニア」というのは、本来あるべき部位から組織が脱出、突出した状態のことを指します。つまり、このヘルニアの状態が腸管に生じると、「鼠径ヘルニア(脱腸)」、椎間板に生じると「椎間板ヘルニア」ということになります。
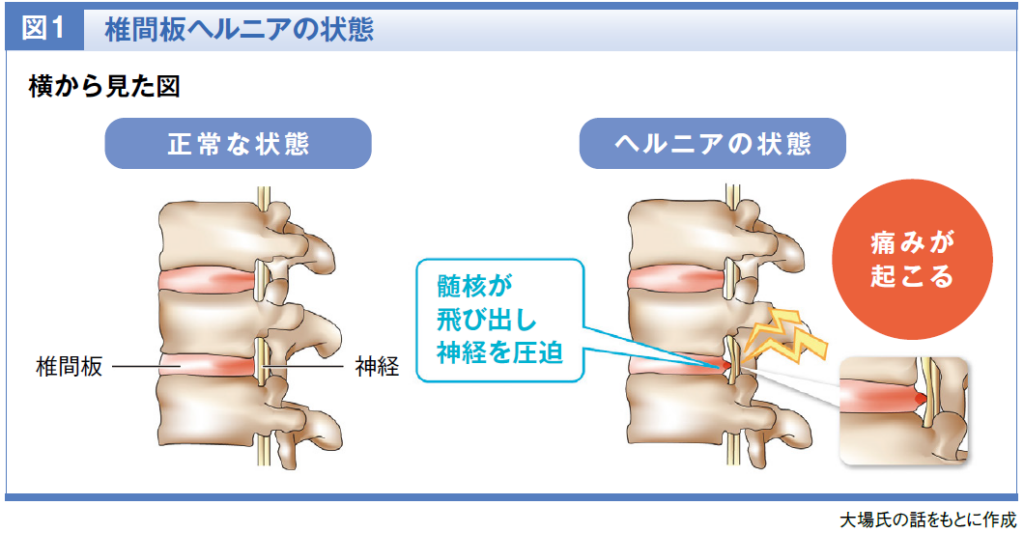
椎間板ヘルニア(図1)は、椎骨の間でクッションの役割を果たす椎間板に負担がかかり、椎間板の中心にある髄核という組織が、その周囲を覆う線維輪を破って脊柱管内に飛び出した状態です。多くの場合、脊椎の後方(背側)に脱出しますので、後方に走行する神経を圧迫することにより痛みや痺れが発生します。
ヘルニアの部位により異なる神経症状
椎間板ヘルニアは、腰を曲げたり反らしたりする動作で負担がかかりやすい下位腰椎や、第4腰椎と第5腰椎の間と第5腰椎と第1仙椎の間 (L5/S1) の椎間板に発生しやすいと言われています。これにより、座骨神経につながる神経根が障害されやすいことから、椎間板ヘルニアでは、腰の下部や尻、太ももの後ろ、すね、足先などの痛みや痺れといった坐骨神経痛の症状が出現します。腰椎椎間板ヘルニアの症状としては、腰痛と片側の下肢痛、痺れなどの神経症状が代表的です。
ただし、椎間板の高位や突出する方向には個人差もあります。稀ではありますが、より上位の腰椎でヘルニアが発生した場合には、大腿神経につながる神経根が障害されるため、太ももの前の方に痛みが出現します。
また、ヘルニアが神経の本管 (馬尾神経) を圧迫してしまうと、激しい腰の痛み、下肢の運動麻痺、および排尿排便障害、殿部、陰部、膀胱、直腸の感覚消失などの馬尾症候群の症状が出現する場合があります。これは緊急で手術を行う必要がある非常に重篤な状態です。
発生機序
椎間板ヘルニアはなぜ起こる?
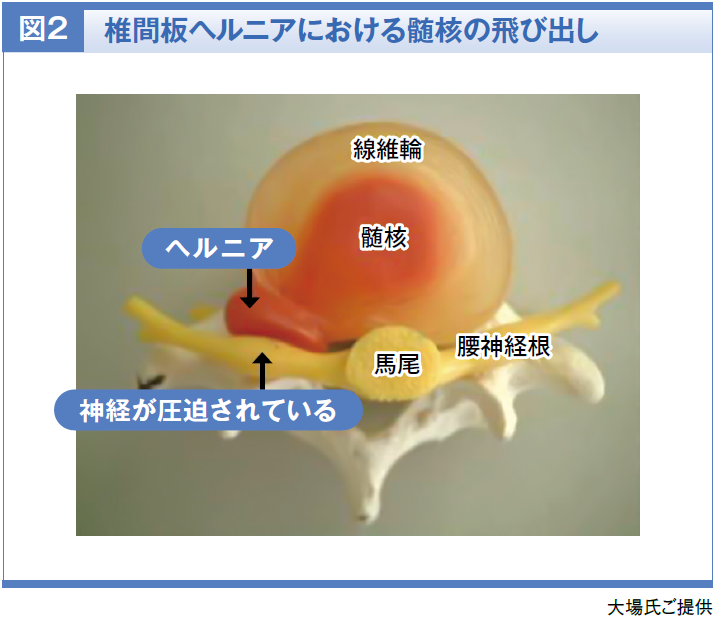
椎間板ヘルニアの発生機序に関しては未解明な部分が多いのですが、現時点で分かっているのは椎間板の二重構造の破綻です。椎間板は1型コラーゲンの組織でできた線維輪の中にゲル状の髄核が入っているのですが、年齢と共に徐々に線維輪が傷み亀裂が入り、その状態で椎間板へ負担がかかるとその亀裂から髄核が押し出されると考えられています(図2)。
好発年齢は壮年期
一般的に多くの疾患は加齢に伴い発症率が高くなることが多いですが、腰椎椎間板ヘルニアはちょうど働き盛りに多く高齢者に少ないという特徴があり、20~40歳代が好発年齢とされています。椎間板の線維輪に変性が加わり、かつアクティブに活動している年代で起こりやすい疾患です。
高齢者で腰椎椎間板ヘルニアが少ない理由としては、加齢に伴い髄核の水分量が減少することが上げられます。高齢者では椎間板自体が潰れて飛び出すものがなくなるため腰椎椎間板ヘルニアは少なくなり、一方で、腰痛の原因として神経の通り道が狭くなる脊柱管狭窄症が多くなります。
【COLUMN】 ぎっくり腰・椎間板ヘルニア・脊柱管狭窄症 その違いは?
一般的に腰痛といえば「ぎっくり腰」が思い浮かぶかと思いますが、椎間板ヘルニアとぎっくり腰はどう違うのでしょうか?
まず、ぎっくり腰は一般的な俗称であり医学用語ではないということを認識しておく必要があります。医学用語としては急激に発生した腰痛全般をさす急性腰痛症にあたります。椎間板ヘルニアは急性腰痛症の一種です。急性腰痛症にはそれ以外にも関節の損傷で起こる腰痛、靱帯や筋肉の損傷で起こる腰痛、そして原因の分からない腰痛などが含まれます。
また、高齢者に多くみられる「脊柱管狭窄症」は、椎間板の突出も一部影響していますが、主に加齢に伴い脊髄の背側にある黄色靭帯が肥厚することにより、神経が通る脊柱管が狭くなることにより徐々に進行する疾患です。椎間板ヘルニアとの大きな違いは、椎間板ヘルニアは前傾姿勢で痛みが増強するのに対し、脊柱管狭窄症は歩行時などの垂直~後傾姿勢で痛みが増幅し、歩行を中断し前傾姿勢で少し休むと痛みが消失する間欠的跛行が特徴的な症状です。
ヘルニアの発生要因
ヘルニアの発生には、日常生活や労働環境などの環境要素と力学的要素、遺伝的要素など多くの因子が複雑に関与しています。一般的に中腰の体勢は椎間板に大きくストレスがかかりますので、力学的に中腰で重いものを持ち上げるなどの作業によりヘルニアが発生しやすいといえます。
ですが、実際に整形外科で診療している中では、中腰で力仕事をしてヘルニアを発症した人が多いかというと必ずしもそうではなく、くしゃみをしてヘルニアが発生する患者さんもいますし、特に思いあたる原因がなくヘルニアが発生する患者さんもいます。おそらく椎間板にかかる負担の積み重ねが発症に関わっていると思われます。
ヘルニアの発生に影響を与える環境的な因子としては、力仕事などの重労働だけでなく長時間座位で過ごす職業の方などではリスクが高くなります(表1)。さらに、トラックの運転手やヘリコプターのパイロットなど、長時間の座位に加えて常に振動を受けているような職業の方ではヘルニア発症のリスクが高いとされています。また、喫煙もリスク因子として上げられており、喫煙量が多いほどリスクが高いとされています。さらに、椎間板ヘルニアには遺伝的にヘルニアになりやすいという家族集積性があることも分かっています。
自然退縮のメカニズム
椎間板ヘルニアは、発症からおよそ3ヵ月で7~8割の患者さんが自然に症状の改善を感じるとされています。これは、「自然退縮」と呼ばれる現象によるものです。
自然退縮は、ヘルニアによる症状の発現とは異なる仕組みで始まります。椎間板ヘルニアの症状は飛び出した髄核が神経を圧迫したり、周囲に炎症を引き起こすことによって現れます。一方、自然退縮は、髄核が本来血流のない椎間板の内側から外に露出し、血流のある組織と接触することがきっかけです。
血液に触れた髄核は異物として認識され、免疫システムによる炎症反応が引き起こされます。この過程で、マクロファージをはじめとする免疫細胞が集まり、炎症性サイトカインのTNF-αが産生されます。さらに、血管新生を促すVEGF(血管内皮増殖因子)などの物質も誘導され、ヘルニア周囲に新たな血管が形成されます。
新しくできた血管を通じて、椎間板の成分を分解する酵素「マトリックスメタロプロテアーゼ(MMP)」が活発に産生されます。MMPには分解する基質や構造の違いにより多くの種類がありますが、その中で特にMMP-3とMMP-7は、髄核の主成分であるプロテオグリカンを効率よく分解できることが分かっており、ヘルニアの縮小に大きく関与しています。
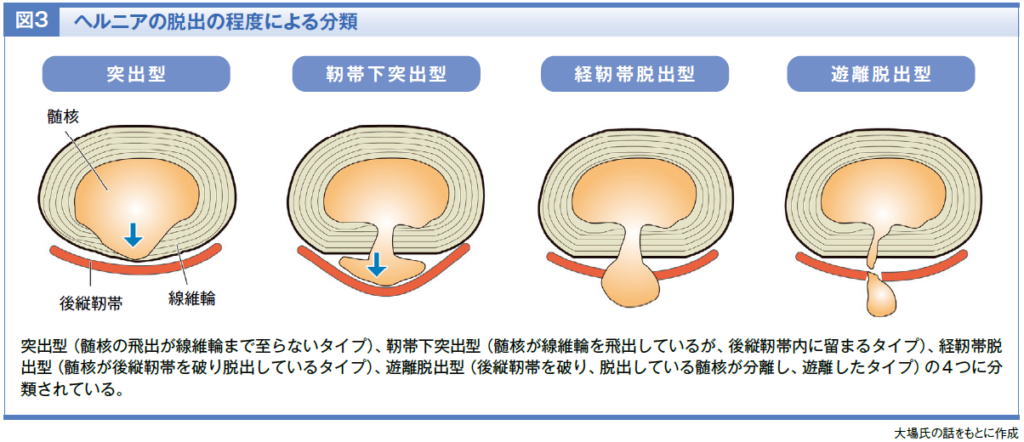
自然退縮が起こりやすいのは、椎間板の髄核が後縦靭帯(背骨の後ろ側にある靭帯)を突き破って外に出ているタイプや、完全に分離している「遊離型」のヘルニアです。一方で、髄核が突出しているだけで靭帯を破っていないタイプや、膨らんでいるだけの「膨隆型」では、退縮が起こりにくいことも明らかになっています(図3)。
神経障害の程度を確認
椎間板ヘルニアの診断では、腰椎のどこにヘルニアが発生し、どの神経が障害されているかを確認していきます。この際、最も重要なのは神経障害の程度を把握することです。特に、排尿や排便がうまくできなくなるといった「馬尾神経」の障害による症状(馬尾症候群)がみられる場合は、注意が必要です。下肢の運動麻痺などの重度の神経障害がある場合には早急な手術を要することもあります。
● 身体所見
下肢の運動麻痺については、たとえば足首を上に上げる力に左右差がある場合や、片側の太ももを伸ばす筋肉だけが弱っている場合など、麻痺が発現している部位と機能ごとに障害されている神経の種類がある程度は明らかになっています。そのため、下肢筋力テストを行って、それぞれの筋肉の機能を評価していきます。加えて、下肢伸展挙上テストや大腿神経伸展テストなどの疼痛誘発テスト、さらに深部腱反射の確認によって、神経根障害があるかどうかを判断していきます。
● 単純X線像
単純X線像には椎間板は映りません。椎骨間(椎間板腔)が狭くなっている部位が確認できる程度です。また、椎間板腔が狭いからといって、必ずしもヘルニアが存在するということではありませんので、単純X線像は椎間板ヘルニアの診断に有用とはいえませんが、MRI撮影を行う前に単純X線像で骨に大きな異常はないかなど、他疾患との鑑別を行います。
● MRI
単純X線像で他疾患との鑑別を行った上で身体所見から椎間板ヘルニアが疑われた場合にはMRI撮影を行います。MRIでは軟部組織も描出できますので、ヘルニアの部位と脱出の程度を把握することができます。
治療の基本は保存的治療
前述の通り、腰椎椎間板ヘルニアの7~8割の患者さんでは、3ヵ月程で自然退縮により症状が軽快することが分かっています。膀胱直腸障害や著明な下肢筋力低下などが見られるような重症例でなければ、自然退縮を待つというのが治療の基本になります。しかし、3ヵ月間痛みや痺れがありますので、症状緩和のための保存的治療(薬物療法、注射療法)を行います。
神経根の炎症による化学的刺激が強い急性期(発症後1~2週間)は、安静が基本となります。少なくとも無理な運動や重量物の搬送などのアクティブな活動をさけてもらうように指導し、炎症を鎮静化させていきます(表2)。
薬物療法で痛みを緩和
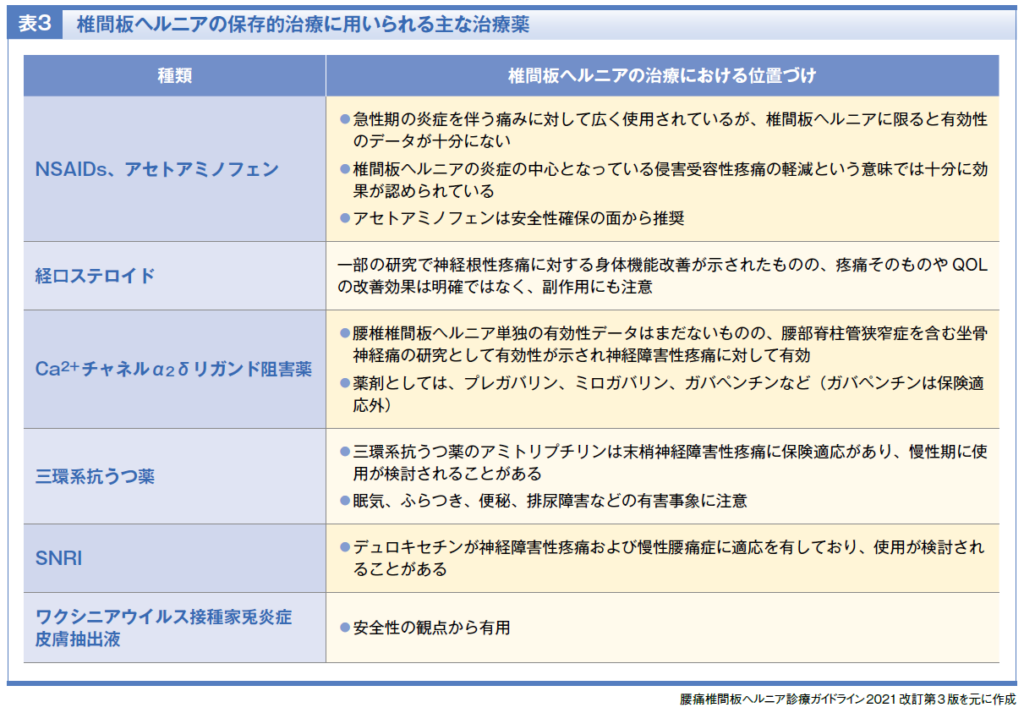
ここで、2021年に改訂された「腰椎椎間板ヘルニア診療ガイドライン改訂第3版」に基づく情報を整理します。
非ステロイド性抗炎症薬(NSAIDs)は、急性期の炎症を伴う痛みに対して広く使用されていますが、椎間板ヘルニアに限ると有効性のデータが十分にあるとはいえません。一方で、椎間板ヘルニアの炎症の中心となっている侵害受容性疼痛の軽減という意味では十分に効果が認められています。アセトアミノフェンは安全性確保の面から推奨されます。
また、経口ステロイドについては、一部の研究で神経根性疼痛に対する身体機能改善が示されたものの、疼痛そのものやQOLの改善効果は明確ではなく、副作用にも注意が必要です。
Ca2+チャネルα2δリガンド阻害薬は、腰椎椎間板ヘルニア単独の有効性データはまだないものの、腰部脊柱管狭窄症を含む坐骨神経痛の研究として有効性が示されていて、神経障害性疼痛に対して有効と考えられています。Ca2+チャネルα2δリガンド阻害薬の薬剤としては、プレガバリン、ミロガバリン、ガバペンチンなどがあります(ガバペンチンは保険適応外)。
三環系抗うつ薬のアミトリプチリンは末梢神経障害性疼痛に保険適応があり、慢性期に使用が検討されることがありますが、眠気、ふらつき、便秘、排尿障害などの有害事象への注意が求められます。SNRIの中ではデュロキセチンが神経障害性疼痛および慢性腰痛症に適応を有しており、使用が検討されることがあります。今後椎間板ヘルニアについても効果検証が期待されます。
安全性の観点からはワクシニアウイルス接種家兎炎症皮膚抽出液が有用で、これも今後のさらなる効果検証が待たれます。このほか、弱オピオイドのトラマドール製剤も、症状や患者背景によっては選択肢となる場合があります(表3)。生物学的製剤は推奨されていません。
実臨床として、当施設では基本的にはNSAIDsやアセトアミノフェンなどの非ステロイドの経口消炎鎮痛薬とCa2+チャネルα2δリガンド阻害薬を用いて鎮痛を試み、それでも痛みが緩和できないような場合にそれ以外の薬剤を用いていきます。副作用の面から、三環系抗うつ薬やSNRIよりも、ワクシニアウイルス接種家兎炎症皮膚抽出液を優先的に投与しています。三環系抗うつ薬やSNRIを使用する場合は、少量から徐々に反応を確認しながら使用していきます。
薬物療法でもとれない痛みに注射療法(ブロック注射)
経口薬による保存的治療を行っても十分な鎮痛作用が得られない患者さんに対してはブロック注射が行われることがあります。薬剤としては、副腎皮質ステロイドや局所麻酔薬、あるいは両方の薬剤を混合したものを用います。
椎間板ヘルニアに対して行われるブロック注射には、硬膜外ブロックや仙骨裂孔ブロック、神経根ブロックがあります。硬膜外ブロックと仙骨裂孔ブロックは、ターゲットを決めずに神経の周りに薬剤をいき渡らせる方法で、外来で行うことが可能です。
一方、神経根ブロックは入院で実施する治療です。仙骨裂孔ブロックや硬膜外ブロックで痛みの改善がみられない場合や、手術に踏み切るかどうか迷っているような患者さんに対して実施します。造影剤を注入し、レントゲンで神経の走行を確認しながら障害されている神経根に針を進め、再現痛を確認した上で薬剤を注入します。
手術療法
絶対的適応と相対的適応
膀胱直腸障害や重度の下肢麻痺は絶対的手術適応であり、手術を急ぐ必要があります。それ以外で手術の導入を検討する例としては、3ヵ月以上にわたる保存療法が無効な症例(自然退縮にいたらない症例)が挙げられます。
また、椎間板ヘルニアは働き盛りの年代で多い疾患であることから、社会的な理由から手術を選択する場合もあります。ひどい麻痺はないものの痛くて動けないが、安静にして自然退縮を待つ時間的余裕はないという場合や、プロのスポーツ選手で少しでも早く痛みを取ってスポーツに復帰したいなどの場合には早期に手術を選択することになります。ただし、そのような患者さんでも手術の予定を待っているうちに自然退縮が進行して症状が軽快するということも往々にしてあります。
手術は、神経を避けてヘルニア部分を切除する椎間板ヘルニア摘出術が最もポピュラーな術式です。それを顕微鏡下と内視鏡下のいずれで行うのか、さらに椎間板へのアプローチ法など、多くの術式が考案されています。この他、ヘルニアが発生している部位の椎間板全体の量を減らし、神経の圧迫を解除する「髄核摘出術」なども選択肢のひとつです。
手術療法は保存療法と比べて短期的な優位性が示されていますが、長期予後になるとその差は減少します。また、手術を施行したとしても10%程度に再発(再脱出)があると言われています。
保存的治療と手術の中間的位置づけ
椎間板酵素注入療法(椎間板髄核融解療法)
「椎間板酵素注入療法」は、保存的治療と手術療法の中間的な位置づけといえる治療法です。ヘルニアの自然退縮では、炎症性細胞からプロテオグリカンなどの椎間板成分を分解する酵素が産生されることで、髄核の縮小が進みます。薬剤注入によって、これと同様の状態を目指すのが椎間板酵素注入療法です。
椎間板酵素注入療法に用いられる薬剤は、コンドリアーゼ(ヘルニコア)です。コンドリアーゼは、ある種の土壌細菌由来の酵素で、髄核の主な成分であるプロテオグリカンを構成するグリコサミノグリカン(主にコンドロイチン硫酸)を特異的に分解し、プロテオグリカンの保水能を低下させることで椎間板内圧を低下させます。それによりヘルニアによる神経根圧迫を軽減させ症状を改善させるという治療法です。
手技的にヘルニア塊に直接薬剤を注入するのは難しいため、椎間板内の髄核に薬剤を注入し、ヘルニア塊を含む髄核全体の体積を減らすことで、神経への圧迫を軽減します。
ただし、コンドリアーゼは異種タンパクであり、再投与によりアナフィラキシーなどの重篤なアレルギー反応を起こす可能性があるため、生涯に一度のみの投与しか行うことができません。
新規治療法開発の可能性
椎間板酵素注入療法は、自然退縮を待つのではなくその状態を人工的に作る治療法であり、いわばヘルニアを直接的に治療する手段であるといえます。しかし前述の通り、コンドリアーゼは抗体産生のために生涯で1回しか投与できない治療法です。今後の目標としては抗体ができない治療法の開発が求められます。
そこでわれわれが着目したのがヘルニアの自然退縮の過程で中心的な役割を果たす酵素 「MMP-7」です。山梨大学では産学共同でヒト型組み換え蛋白MMP-7(ヒトリコンビナントMMP-7)を主成分とする新規の化学的髄核融解療法を開発し、2022年2月から医師主導治験を開始しています。治験は現在も継続中で今後の解析結果が期待されている状況です。
また複数の研究機関で椎間板の再生医療の研究も進められています。再生医療の実現にはまだ時間がかかると思われますが、研究の進展に期待したいところです。
椎間板ヘルニア診療における薬剤師の役割
椎間板ヘルニアの診療において薬剤師に期待することは、やはり薬物療法に関する患者指導と副作用の管理です。椎間板ヘルニアの神経障害性疼痛に対して、ガバペンチンやプレガバリン、ミロガバリンといったCa2+チャネルα2δリガンド阻害薬は第一選択薬剤です。しかし一方ではこれらは、中枢神経系に作用して痛みを緩和する薬剤のため、眠気や吐き気など中枢神経系の副作用の出現が気になります。整形外科の診療現場では、徐々に用量を増やして投与することが多くあり、投与時に患者さんには車の運転などには注意するように伝えるのですが、薬局でも繰り返し指導してもらえれば非常に助かります。
また、ひとくちに腰痛といっても原因は多岐にわたります。壮年期で、発症が急激、腰痛だけでなく片側の下肢痛があれば、椎間板ヘルニアの可能性が高くなります。もしもその他の疾患で薬局に来ている患者さんで腰痛で下肢に痛みや痺れがあれば、それは病院を受診した方がよい腰痛であるといえますので、受診勧奨をしてもらえたらと思います。
大場 哲郎 氏
2003年山梨大学医学部卒業、2008年同大学大学院修了。山梨大学整形外科学講座を経て、2012年米国ヴァンダビルト大学整形外科に客員准教授として留学。2021年より山梨大学大学院整形外科学講座講師。JASA (Japan Association of Spine surgeons with Ambition) 主メンバー、日本腰痛学会評議委員、日本側弯症学会国際委員会・学校検診委員会委員(2021年~)、Bio Spine Japan幹事、脊椎脊髄病学会評議委員(2024年~)。腰椎椎間板ヘルニア診療ガイドライン第3版改訂委員。