監修
国立がん研究センター東病院 総合内科科長 先端医療科/腫瘍内科
内藤 陽一 氏
乳がんは日本人女性の部位別がん罹患数第1位の疾患であり、年間約9.9万人の女性が新たに乳がんを発症しています。治療法の発展により比較的治療成績は良好ではあるものの、いまだ年間15,000人が乳がんにより命を落としています。さらなる治療法の開発が進む乳がん治療の基礎から最新の治療薬までを、国立がん研究センター東病院 総合内科科長、先端医療科/腫瘍内科の内藤陽一氏に解説いただきました。
日本人女性の9人に1人が乳がんを発症
乳がんは、日本人女性の9人に1人が罹患するといわれています。乳がんの罹患率は増加傾向にあります。その原因としては食生活の欧米化に伴い日本人の体質が変化していることが考えられています。一般にがんは高齢者に多く見られますが、乳がんは40〜50代での発症も比較的多いことが特徴です。
また、乳がんの重要な危険因子として、エストロゲンへの曝露期間が挙げられます。初潮が早い人や閉経が遅い人ではエストロゲンに曝露される期間が長いのですが、それが乳がんになりやすい要因の一つとも考えられています。その他にも、出産経験の有無、遺伝的要因、肥満、思春期の高身長、アルコール摂取などがリスク因子として知られています。
発見のきっかけとして多いのは自覚症状です。乳房のしこりや、乳頭・乳輪部の湿疹・ただれ、乳頭からの異常分泌、乳房のくぼみなど、乳房の変化に気づいて受診し、発見されることが多くなっています。また、乳がん検診によって、無症状の段階で発見されるケースも増加しています。
確定診断とともに乳がんの悪性度を評価
診断では、まず視触診、マンモグラフィー、エコー、MRIなどを実施し、乳がんが疑われた場合は針生検などによる組織診を行い、確定診断に至ります。また、これらの検査結果から、組織型(表1)、腫瘍の大きさ、リンパ節・遠隔転移の有無に加え、がん細胞におけるホルモン受容体(エストロゲン受容体およびプロゲステロン受容体)やHER2の発現、増殖能を示すKi67陽性細胞の割合※などを評価します。
※Ki67陽性細胞の割合が高い乳がんは増殖能が高く、悪性度が高いとされる
ステージ(病期)とサブタイプの評価
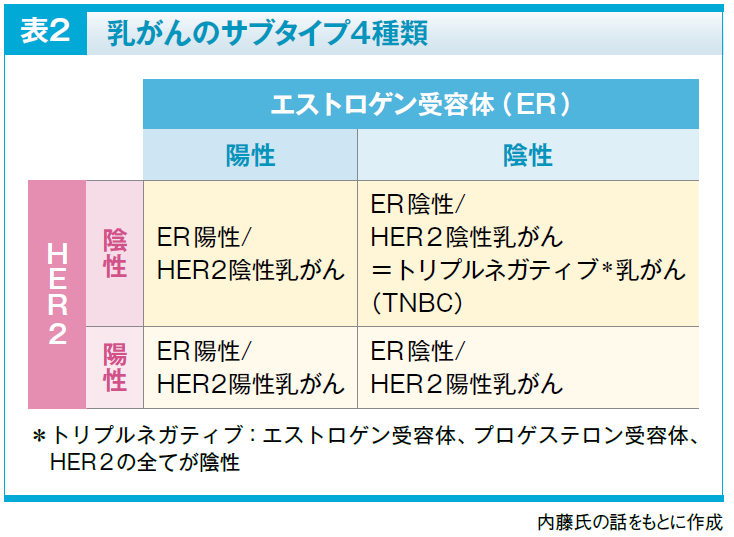
さらに、ステージと治療方針の決定に重要となるサブタイプの判定を行います。病巣の大きさや広がりなどの乳がんの状態(T)、リンパ節転移の有無と範囲(N)、遠隔転移の有無(M)のTNM因子を元にステージの評価を行い、がん細胞のホルモン受容体とHER2発現の有無によりサブタイプを判定します(表2)。
治療の種類
乳がんの治療には、手術、薬物療法(ホルモン療法、化学療法、分子標的薬、免疫チェックポイント阻害薬)、放射線療法、緩和医療などがあります。
手術療法
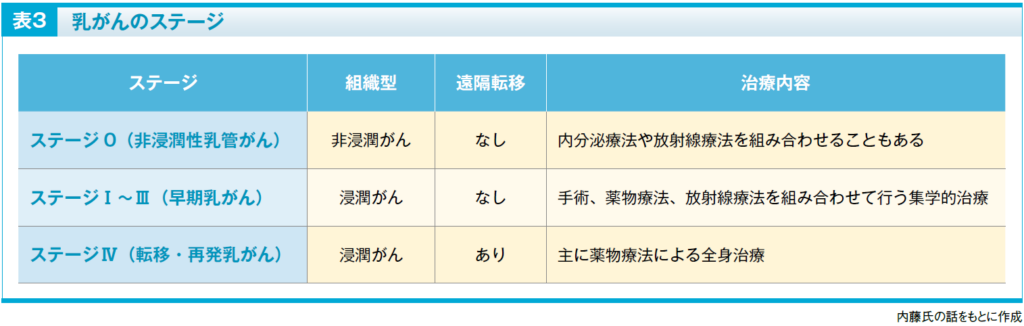
ステージ0〜Ⅲの乳がんの治療は、手術による切除が基本となります(表3)。手術の方法には、以下のようなものがあります。
●乳房温存術(乳房部分切除術):がん細胞が遺残しないように、腫瘍とその周囲の正常乳腺を切除する方法です。通常、温存乳房に放射線療法が加えられます(乳房温存療法)。
●乳房全切除術:乳管やリンパ管に沿って広がる乳がんを取り残さないように、乳房全体を切除します。
●リンパ節に対する手術:乳がんは腋窩リンパ節に転移しやすいため、必要に応じて、腋窩リンパ節郭清術(腋窩リンパ節と周囲の脂肪組織を切除する手術)や、がん細胞が最初に到達するセンチネルリンパ節を切除し転移の有無を確認するセンチネルリンパ節生検が行われます。通常、センチネルリンパ節生検でがんの転移がなければ、腋窩リンパ節郭清は行いません。
ホルモン療法
乳がんのがん細胞の多くは、女性ホルモンが栄養源となって増殖するため、がん細胞にホルモン受容体が出現しているタイプの乳がんの場合は、ホルモン療法によりその働きを阻害することでがんの増殖を抑制していきます。ホルモン療法には主に表4の薬剤が用いられ、閉経前と閉経後で分けて薬剤が選択されます。
化学療法
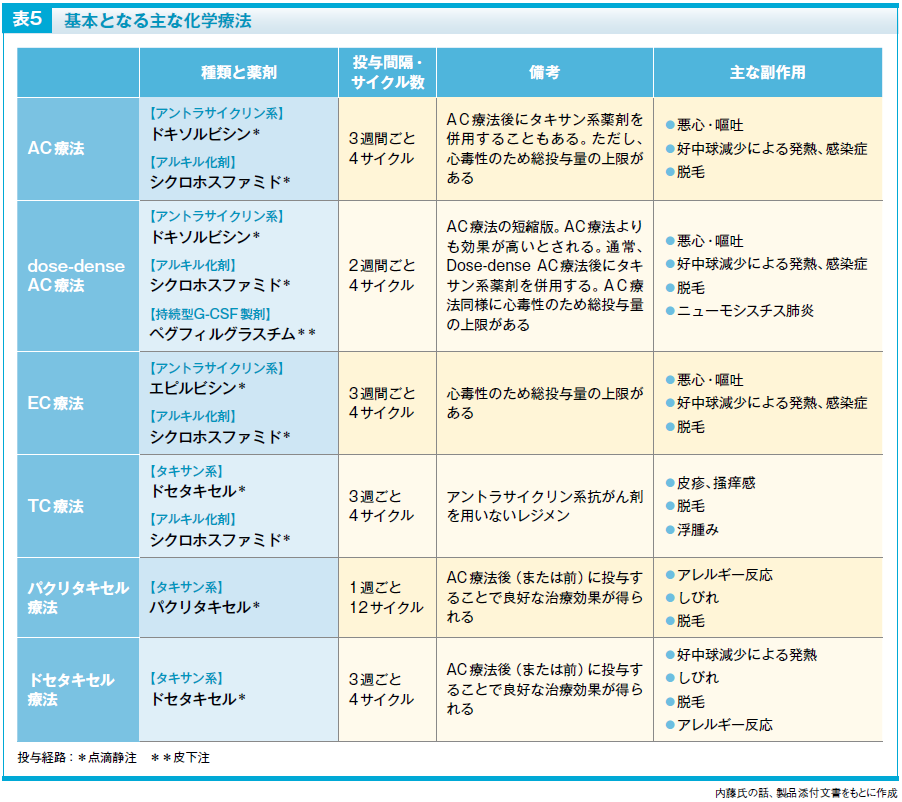
乳がんの化学療法では、アントラサイクリン系とタキサン系の抗がん剤を用いた化学療法が治療の基本となることから、AC療法やEC療法、パクリタキセル療法、ドセタキセル療法などが選択されることが多くなります。その他にも手術可能な早期乳がんの治療で多く用いられる化学療法を表5に示します。
最近は、術前に化学療法を行い、病巣を小さくすることで乳房の温存が可能となること、術前化学療法の効果によって術後の治療を変えることができることなど、その後治療選択肢が広がることから、術前に化学療法を行ってから手術を行うケースが多くなってきています。
分子標的薬
乳がんの治療には分子標的薬も用いられます。特に広く使用されるのが抗HER2療法に用いられるトラスツズマブとペルツズマブです。抗HER2療法では、基本はトラスツズマブを用い、再発リスクが高い症例ではペルツズマブが併用されます。抗HER2薬はドセタキセルまたはパクリタキセルとの併用で使用します。抗HER2薬としては、抗体薬物複合体(ADC)であるトラスツズマブ エムタンシンや、トラスツズマブ デルクステカンも使用されます。
また、トリプルネガティブ乳がんでは、免疫チェックポイント阻害薬であるペムブロリズマブとアテゾリズマブが使用できます。ペムブロリズマブは術前から化学療法とともに使用され、転移・再発でもPD-L1陽性の場合に化学療法と併用で使用されます。同じく免疫チェックポイント阻害薬であるアテゾリズマブは、トリプルネガティブの転移・再発乳がんでPD-L1陽性例で使用可能な薬剤ですが、術前や術後には使用されません。
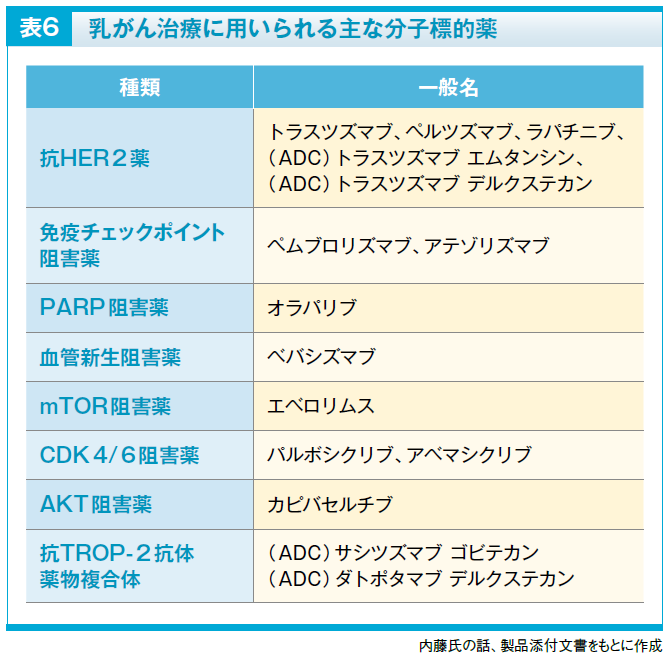
その他にも血管新生阻害薬、PARP阻害薬、mTOR阻害薬、AKT阻害薬、CDK4/6阻害薬などが、主に転移・再発乳がんの治療に用いられています。CDK4/6阻害薬は、ホルモン受容体陽性・HER2陰性の進行・再発乳がんで、ホルモン療法と併用して使用されています(表6)。
緩和的治療
身体的・精神的な苦痛を和らげ、患者とその家族のQOLを向上させることを目的とした医療です。転移・再発乳がんは根治が難しく、薬物療法を中心に、がんによる症状の緩和、症状出現の先送り、生存期間の延長を目標に治療を行います。しかし、薬物療法の効果が十分期待できない場合や有害事象の懸念などから、病状が進行した場合は特に、緩和医療に専念していくことが勧められるようになります。
治療方針の決定
実臨床で治療方法の選択は、おもにステージとサブタイプから判断します。
ステージの観点からは、浸潤のないステージ0の非浸潤性乳管がんは、手術による局所療法、ステージⅠ〜Ⅲの早期乳がんに対しては、手術と薬物療法、放射線療法を組み合わせた集学的治療を行います。
どの薬物療法にするかは、エストロゲン受容体(ER)およびHER2の陽性・陰性の組み合わせによる4つのサブタイプが基本的な選択の基準です。大まかには、ERが陽性の場合はホルモン療法が有効なため、ホルモン療法が組み合わされます。HER2陽性の乳がんでは抗HER2療法を実施します。化学療法は全てのサブタイプに用いられます(表7)。トリプルネガティブの場合、免疫チェックポイント阻害薬の対象になります。
一方、ステージⅣの転移・再発乳がんは根治的な手術の対象にはならず、基本的には薬物療法や緩和医療により症状の管理および生存期間の延長を目指します。
早期乳がんのサブタイプごとの治療の実際
1.エストロゲン受容体陽性/HER2陰性
もっとも患者数が多いサブタイプで全体の約70%を占めます。このサブタイプはさらに異型度が低く増殖力の弱いluminal Aタイプと、異型度が高く増殖力の強いluminal Bタイプに亜分類されます。治療は手術とホルモン療法が基本となりますが、再発リスクに応じて化学療法も施行していきます。
化学療法としては、再発リスクが低い場合にはタキサン系抗がん剤だけを用いるTC療法+ホルモン療法で治療することもありますが、基本はアントラサイクリン系とタキサン系の抗がん剤を使うAC療法やdose-dense AC療法、またはEC療法のいずれかを行い、その後にパクリタキセル療法またはドセタキセル療法+ホルモン療法が選択されることが多くなります。最近では、化学療法を行うかどうかの判断に、多遺伝子アッセイが用いられることが多くなっています。多遺伝子アッセイはアントラサイクリン系抗がん剤を使用するかどうかの判断にも参考にされることがあります。
2.エストロゲン受容体陰性/HER2陽性
HER2陽性の場合、抗HER2療法と化学療法が治療の基本となります。病巣が小さい場合には先に手術を行い、術後にトラスツズマブを用いた抗HER2療法とパクリタキセル療法を行うこともありますが、基本的には術前から化学療法+トラスツズマブ・ペルツズマブ併用の抗HER2療法を開始することが多くなります。
化学療法はアントラサイクリン系の抗がん剤を用いるAC療法やEC療法を施行し、その後に抗HER2療法としてトラスツズマブ+ペルツズマブと、ドセタキセル療法またはパクリタキセル療法を行う治療法がよく行われます。術前薬物療法の効果によって術後に行う薬物療法を決定するresidual disease-guided approach(残存病変に基づく治療)も行われます。
3.エストロゲン受容体陽性/HER2陽性
HER2とホルモン受容体の両方が陽性のトリプルポジティブのタイプでは、前項のホルモン受容体陰性/HER2陽性のサブタイプと同じ化学療法と抗HER2療法を行い、それに加えてホルモン療法を行います。AC療法またはEC療法の化学療法→抗HER2療法(トラスツズマブ+ペルツズマブ)+ドセタキセル療法またはパクリタキセル療法を行い、化学療法後にホルモン療法も行います。
4.エストロゲン受容体陰性/HER2陰性(トリプルネガティブ)
トリプルネガティブは他のサブタイプより治療成績が悪いと報告されています。腫瘍の大きさが2cm以上あるような再発リスクが高い症例では、術前から抗がん剤と免疫チェックポイント阻害薬ペムブロリズマブを用いた治療を行います。化学療法のレジメンとしては、カルボプラチン/パクリタキセル療法+ペムブロリズマブを施行した後、ペムブロリズマブ+AC療法またはEC療法を施行し、術後はペムブロリズマブを半年継続するというのが基本的な治療となっています。
新規の乳がん治療薬:抗体薬物複合体(ADC)
近年、がん治療の新たな選択肢として、抗体薬物複合体(Antibody drug conjugate: ADC)が大きく注目を集めています。ADCはがん細胞特有の分子を標的とする抗体にリンカーを介して抗がん剤(ペイロードと呼びます)を結合させたバイオ医薬品です。
従来の抗がん剤は、抗腫瘍効果は高いものの、正常細胞も攻撃してしまうなど細胞選択性に乏しいという課題がありました。一方で、近年がん治療に用いられている各種分子標的薬は、がん細胞特有の分子を標的とするため選択性は高いものの、単一の分子だけを治療ターゲットとするため、抗腫瘍効果が限定的となるケースもあり、治療効果に限界があることが課題とされていました。
そこで開発されたのが、抗体が特定の分子に選択的に結合する性質を利用したADCです。抗がん剤を結合させた抗体ががん細胞に到達し、結合した後に抗がん剤を細胞内で放出することで、強力な抗腫瘍効果を発揮します。つまり、ADCは、がん治療薬に求められてきた高い細胞選択性と強力な抗腫瘍効果の両方を兼ね備えた、革新的な薬剤といえるでしょう。
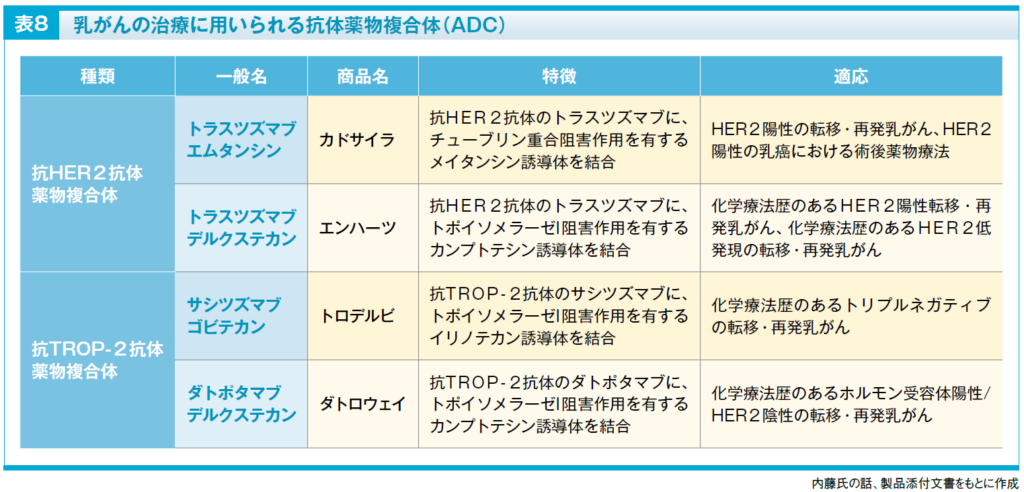
現在、日本では乳がんを対象としたADCが4種類使用可能となっています(表8)。
HER2を標的としたADC
トラスツズマブ エムタンシンと、トラスツズマブ デルクステカンは、いずれもHER2を標的としたADCで、HER2陽性乳がんに用いられます。現時点での適応としては、トラスツズマブ エムタンシンは、HER2陽性の転移・再発乳がんに加えて、手術可能なHER2陽性早期乳がん(ステージⅠ〜Ⅲ)において、術前化学療法後に病理学的完全奏効(pathological complete response: pCR)が得られなかった症例への術後補助療法としても使用可能です。
一方、トラスツズマブ デルクステカンは、HER2陽性の転移・再発乳がんに対する2次治療に加え、サブタイプとしてはHER2陰性に分類されるものの、HER2の低発現(HER2-low)を認める転移・再発乳がんに対しても、化学療法後の乳がんを対象として使用可能です。初回治療としての有効性も示されており、適応拡大が期待されています。
TROP-2を標的としたADC
2024年以降に新しく登場したサシツズマブ ゴビテカンとダトポタマブ デルクステカンは、がんの浸潤や増殖に関与するTROP-2を標的としたADCです。サシツズマブ ゴビテカンは、現在のところトリプルネガティブの転移・再発乳がんの2次治療以降が対象となっていますが、ホルモン受容体陽性/HER2陰性の転移・再発乳がんへの適応拡大も申請されています。一方、ダトポタマブ デルクステカンはホルモン受容体陽性/HER2陰性の転移・再発乳がんに対する2次治療以降として使用可能です。
ADCによる治療の将来的な可能性
現在のところ、TROP-2を標的とするADCは主に転移・再発乳がんに対する2次治療以降で使用されていますが、各薬剤については1次治療や、ステージⅠ〜Ⅲの早期乳がんに対する術前・術後治療としての開発も進められています。今後、転移・再発乳がんだけでなく、早期乳がんの初期治療にもADCが使用可能となれば、再発率を大きく低下させられる可能性があり、乳がんの治療戦略全体が大きく変わることも考えられます。それほどまでに、ADCは乳がん治療を変革し得る革新的な薬剤といえるでしょう。ADCはいずれも高額な薬剤ですが、早期乳がんの手術前後の初期治療で使用できるようになれば、長期的には再発の抑制や治療費削減といった観点から、経済的な効果も期待されます。
乳がん治療における薬剤師の役割
乳がんの薬物療法は非常に複雑です。近年では分子標的薬やADCの登場により、副作用の種類も多様化しています。そのため、副作用のモニタリングの面でも、薬剤師によるサポートは必要不可欠です。さらに、例えば、免疫チェックポイント阻害薬では、副作用として副腎皮質ホルモンの分泌が低下し、副腎不全を引き起こすことがあります。
従来、副腎不全は内分泌の専門医が対応する非常にまれな疾患でしたが、現在ではがん治療の副作用として見られるようになっています。そのため、十分な専門知識を持たない非専門医が治療を担当することもあり、アドヒアランスの重要性、シックデイの対応などきめ細かな対応が難しい場合もあります。がん薬物療法では、このようなケースが少なくありません。薬剤師の皆さんには、副作用として新たに出現した疾患への治療サポートという観点からも、積極的に関与していただきたいと考えています。
内藤 陽一 氏
2000年群馬大学卒業。2011年より国立がん研究センター東病院勤務。2022年より同院総合内科長。腫瘍内科医として、乳がん、GISTを中心に診療に取り組みながら、国内・国際ガイドライン策定などを行い、また薬剤の開発にも取り組んでいる。同時に総合内科として副作用のマネジメントにも取り組んでいる。