監修
独立行政法人国立病院機構 福岡病院 循環器内科 医長
絹川 真太郎 氏
日本では高齢化の進行に伴い心不全患者が増加しており、2030年には130万人に達するという推計もあります1)。心不全マネジメントにおいては、発症予防や再入院予防を柱とした、継続的かつ多職種連携による支援が重視されるようになり、2025年3月には日本の心不全診療ガイドラインも全面的に改訂されました2)。
そこで今回は、改訂された心不全診療ガイドラインの要点、心不全薬物治療の変化、心不全のマネジメントにおいて薬剤師が担う役割などについて、独立行政法人国立病院機構 福岡病院 循環器内科 医長の絹川真太郎氏に解説いただきました。
急性・慢性の区別を削除
一貫したマネジメントの重要性
近年の心不全患者の増加や治療戦略の変化を背景に、日本循環器学会および日本心不全学会は、2025年3月に『2025年改訂版 心不全診療ガイドライン』を発表しました2)。これは、従来の日本の急性・慢性心不全診療ガイドライン3,4)をベースに、最新の海外ガイドラインの内容5-8)や日本における心不全診療の課題をふまえて全面的に見直されたもので、日々の臨床現場に即した指針となるよう作成されています。
今回の改訂では、心不全において「急性期」「慢性期」の定義が明確でないことを考慮し、ガイドラインのタイトルから「急性」「慢性」の表記が削除されました。この変更は、心不全の予後を改善していくうえで、一貫したマネジメントが欠かせないことを示すものです。
心不全リスク・前心不全に対する指針として
「心不全予防」の章を拡充
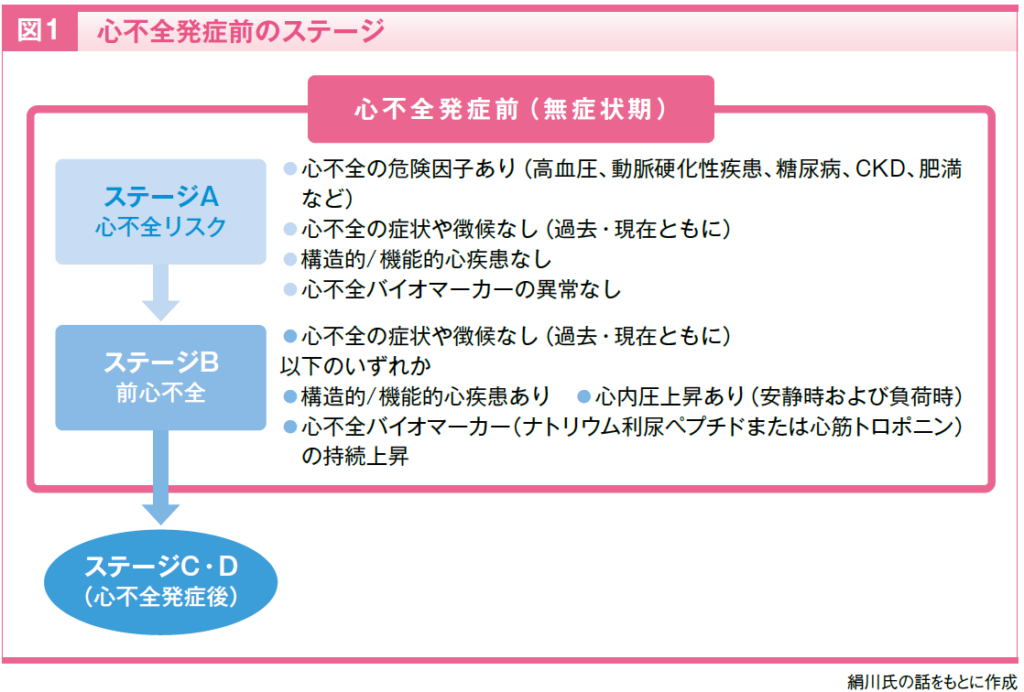
心不全は一度発症すると予後不良であるため、可能な限りその発症を防ぐことが重要です。今回の改訂2)では、予防に関するエビデンスの蓄積を受けて、心不全発症前であるステージA(心不全リスク)およびステージB(前心不全)(図1)に対する指針として「心不全予防」の章を拡充しました。
たとえば、ステージAでは、従来から心不全のリスク疾患として挙げられていた高血圧や糖尿病、動脈硬化性疾患に加え、今回新たに慢性腎臓病(CKD)が加えられました。また、心不全発症予防に向けた生活習慣の改善、基礎疾患に対する薬剤選択の方針など、実践的な推奨も盛り込まれています。近年は、ナトリウム・グルコース共輸送体2(SGLT2)阻害薬やミネラルコルチコイド受容体拮抗薬(MRA)のフィネレノンなど、心不全リスク疾患と心不全の双方に適応がある薬剤も増えており、心不全予防を念頭に置いた薬剤選択の重要性も高まっています。
心不全の分類 HFimpEFが加わる
心不全の治療選択においては、従来から左室駆出率(Left Ventricular Ejection Fraction; LVEF)を指標とした心不全分類が用いられてきましたが、その定義は臨床試験や国によりバラツキがありました。そのため、2021年に日米欧の心不全学会が「Universal definition and classification of heart failure」を提唱し、国際的に統一された心不全分類が導入されました8)。
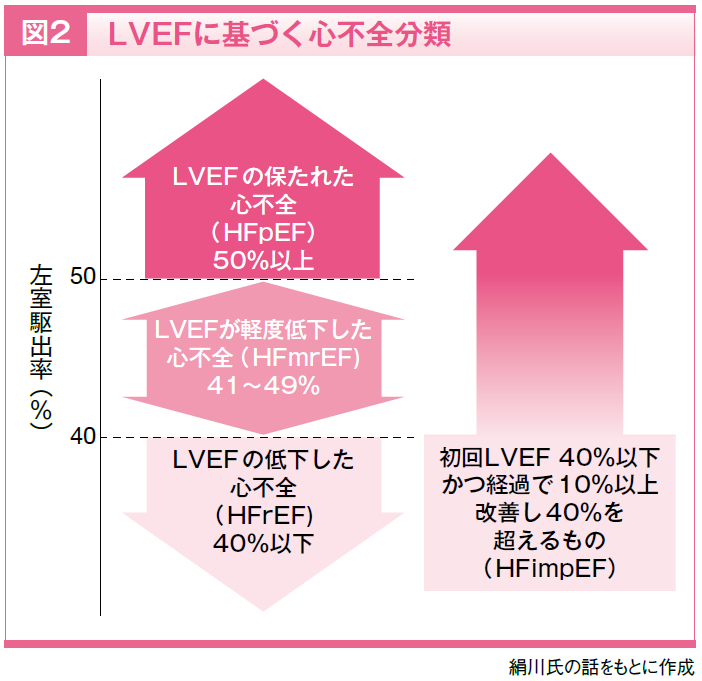
今回の改訂2)では、この国際分類にならい、LVEFを用いた心不全分類を、LVEF 40%以下の「LVEFの低下した心不全(Heart Failure with reduced Ejection Fraction; HFrEF)」、LVEF 41~49%の「LVEFの軽度低下した心不全(Heart Failure with mildly-reduced Ejection Fraction; HFmrEF)」、LVEF 50%以上の「LVEFの保たれた心不全(Heart Failure with preserved Ejection Function; HFpEF)」と変更し、さらに新たにLVEFの経時変化を反映した「LVEFの改善した心不全(Heart Failure with improved Ejection Fraction; HFimpEF)」の定義が加えられました。
HFimpEFは、LVEFが初回40%以下の患者において、治療により10%以上改善し、40%を超えた場合が該当し、HFrEFに対するβ遮断薬投与後などによく経験される病態です(図2)。その予後は比較的良好ですが9-11)、LVEFが改善しても慢性疾患であることに変わりはありません。HFimpEFでの心不全治療の中断が予後悪化の引き金になることも報告されおり12)、HFimpEFという分類の新設は、LVEF改善後の治療継続の重要性も強調しています。ただし、現時点ではHFimpEFに対する標準治療のエビデンスは十分とはいえないため、個々の患者の状態に応じた治療選択が行われています。
HFrEF治療の中心を担う 「ファンタスティック4」
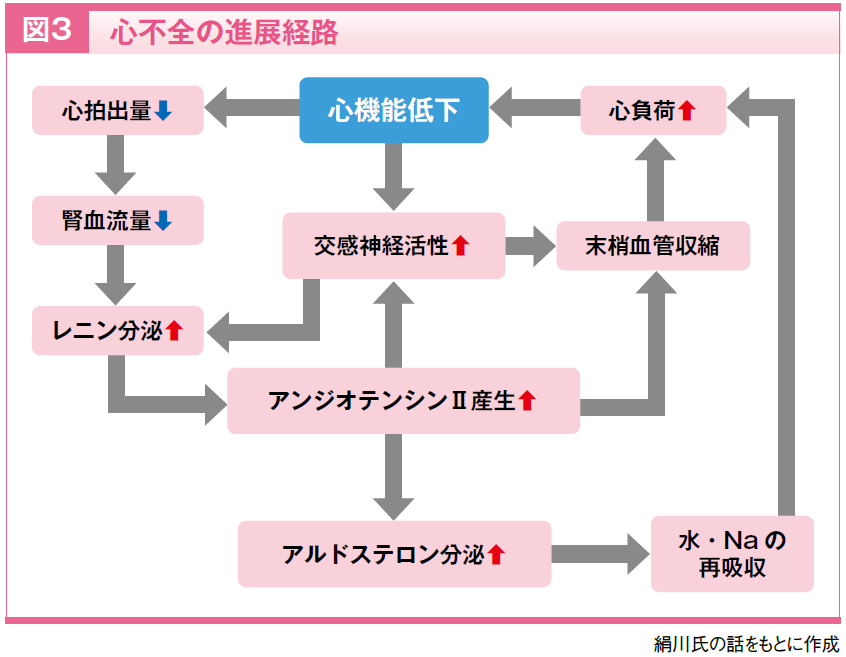
LVEFの低下したHFrEFでは、心筋リモデリングの進行や体液貯留といった病態の進展に、交感神経系やレニン・アンジオテンシン・アルドステロン(RAA)系の過剰な活性化が関与しています(図3)。
そのためHFrEF治療では、これらを抑制するβ遮断薬、アンジオテンシン変換酵素(ACE)阻害薬/アンジオテンシンII受容体拮抗薬(ARB)、MRAが中心的な薬剤として長らく用いられてきました。
その一方で、近年では、アンジオテンシン受容体ネプリライシン阻害薬(ARNI)やSGLT2阻害薬などの薬剤が心不全への適応を取得したことで、HFrEFに対する治療選択の幅が広がりました。今回の改訂2)では、ステージC(症候性心不全)以上のHFrEFに対する基本薬として、β遮断薬、ACE阻害薬/ARB/ARNI、MRA、SGLT2阻害薬の4剤が明記され(「ファンタスティック4」とも呼ばれる)、これらを可能な限り早期から導入し、忍容できる目標量まですみやかに増量していくことが推奨されました(図4)。
● ARNI
ARNIはネプリライシン阻害作用とARB作用を有する薬剤です。ネプリライシンは心保護作用をもつナトリウム利尿ペプチドを分解する酵素であり、ARNIはネプリライシンを抑制することで心不全に対する治療効果を発揮します。
日本のARNIの添付文書では、効能または効果に関連する注意として「アンジオテンシン変換酵素阻害薬又はアンジオテンシンII受容体拮抗薬から切り替えて投与すること」とされていますが13)、今回の改訂2)では、エビデンスや海外での推奨状況を踏まえ、LVEF 40%以下の急性非代償性心不全で血行動態が安定した患者(NYHA心機能分類II~III度)に対して、再入院の抑制を目的としたARNI導入も推奨されました。
なお、ARNIは血圧降下作用が比較的強いため、血圧が低い患者への投与は慎重に検討する必要があり、NYHA心機能分類IV度の重症例への投与は推奨されていません。さらに、ACE阻害薬とARNIはともにブラジキニン分解抑制作用があり、その併用は血管浮腫のリスクを高めます。そのため、ACE阻害薬からARNIに切り替える際には、少なくとも36時間以上の休薬期間を設ける必要があります(表1)。
● β遮断薬
β遮断薬のHFrEFに対する予後改善効果は、多くの臨床試験で確認されており14-16)、ガイドライン2)では、禁忌がなければカルベジロールまたはビソプロロールの投与が推奨されています。
β遮断薬は、うっ血のコントロール後に少量から開始し、忍容性を確認しながら段階的に目標量まで増量します。ガイドライン上は速やかな増量が勧められていますが、重度の心機能障害がある患者などでは、急な増量によって血行動態が不安定となって治療継続が難しくなることもあります。効果には用量依存性があるため最大目標量での投与が望まれますが、ある程度の時間をかけて増量しなければならない患者も存在します。
● MRA
MRAは、腎機能や血清カリウム値に問題がなければ、比較的導入しやすい薬剤です。ガイドライン2)では、NYHA心機能分類II~IV度(LVEF 40%以下)の患者に対して、スピロノラクトンおよびエプレレノンの投与が推奨されています。用量依存性はあまりありませんが、海外エビデンスの多くは低用量(スピロノラクトン25mg/日、エプレレノン50mg/日)での検証によるものであり、標準用量範囲内での効果に基づく知見です。
MRA投与中には血清カリウム値の上昇に注意が必要ですが、血清カリウム値5.0~5.4mEq/L程度であれば、ただちに休薬するよりも、食事からのカリウム摂取制限などを行いながら投与を継続することが望まれます。また、カリウム上昇作用や腎毒性のある薬剤(非ステロイド性抗炎症薬など)の減量や中止、必要に応じてカリウム低下薬の併用も検討します。
● SGLT2阻害薬
もともと糖尿病治療薬として開発されたSGLT2阻害薬ですが、HFrEF患者を対象とした大規模臨床試験でも予後改善効果が明らかとなり17-19)、今回の改訂2)では、糖尿病の有無にかかわらず、症候性のHFrEFの心血管死および心不全入院の抑制を目的とした投与が推奨されました。SGLT2阻害薬の心不全に対する有効性には、複数の機序が関わっていると考えられていますが20)、血行動態に大きな影響を与えずに利尿作用を発揮し、早期からの投与でうっ血解除にも寄与します。
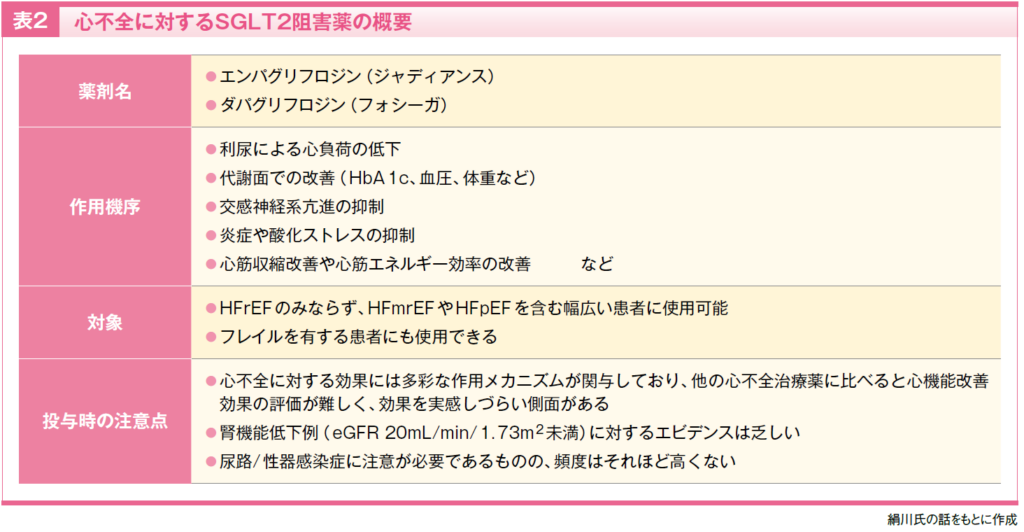
なお、SGLT2阻害薬の投与にあたっては、ナトリウム利尿亢進や血管内脱水による起立性低血圧症状、尿路・性器感染症などの副作用に注意が必要です。フレイル合併例や低体重の患者においても一定の有効性が報告されているものの21-23)、作用機序を踏まえた慎重な観察を心がける必要があります(表2)。
ファンタスティック4以外の薬剤の位置づけ
HFrEFに対する薬物治療では、エビデンスに裏付けられたファンタスティック4による標準治療が基本となりますが、近年は新たな治療選択肢も登場し、個々の病態に応じて併用が検討されます。
● イバブラジン
イバブラジンは、洞結節にある過分極活性化環状ヌクレオチド依存性(HCN)チャネルを阻害し、心拍数を抑制する薬剤です。ガイドライン2)では、最大耐用量のβ遮断薬を含む標準治療にもかかわらず、NYHA心機能分類II~IV度のHFrEF患者(LVEF 35%以下)で、かつ洞調律で心拍数75回/分以上の場合に、心血管死または心不全入院の抑制を目的として追加投与の検討が推奨されています。β遮断薬では心収縮能低下や血圧低下をきたしうる一方、イバブラジンはそれらが生じにくく、β遮断薬を十分量にできない場合の補完として用いられます。
● ベルイシグアト
ベルイシグアトは、可溶性グアニル酸シクラーゼ(sGC)刺激薬で、環状グアノシン一リン酸(cGMP)の産生を促します。心不全ではNO-SGC-CGMP経路が障害されるため、血管拡張や心筋保護作用が減弱していますが、ベルイシグアトによるcGMP産生促進によりNO-SGC-CGMP経路が活性化され、心不全進展抑制効果をもたらします。
ガイドライン2)では、十分な標準治療にもかかわらず心不全増悪をきたしたNYHA心機能分類II~IV度のHFrEF患者(LVEF 45%未満)に対して、心血管死または心不全入院の抑制を目的として投与を考慮することが推奨されています。ARNIなどとの併用も可能であり、血圧低下の副作用は少ないことから、NYHA心機能分類IV度など重症例に対しても投与が可能です。
SGLT2阻害薬が治療の柱に
これまで、HFpEFやHFmrEFにおいては、予後改善の明確なエビデンスを有する薬剤が存在せず、利尿薬によるうっ血コントロールや原疾患に応じた治療が行われてきました。HFpEF/HFmrEF患者は、高血圧、心房細動、CKDなど心不全リスクとなる疾患を抱えていることも多く、心臓以外の要因が心機能に影響を与えているケースも少なくありません。
そうしたなか2021~2022年になると、LVEFが40%以上の心不全患者を対象に行われた大規模な国際共同第III相臨床試験において、SGLT2阻害薬が心不全による入院、心血管死、心不全増悪を有意に抑制することが報告されました24,25)。心機能が比較的維持されたHFpEF/HFmrEF患者で予後改善効果が得られたという結果は、SGLT2阻害薬が心臓に対する直接的作用だけでなく、代謝や循環動態などの改善を介して、心不全の病態を改善していることを示していると思います。
こうしたエビデンスを踏まえ、今回の改訂2)では、症候性HFmrEF/HFpEF患者すべてに対し、禁忌がない限りエンパグリフロジンまたはダパグリフロジンの投与が推奨されました2)。
糖尿病・CKD合併例では非ステロイド性MRAも選択肢
非ステロイド型MRAであるフィネレノンは、LVEF 40%以上の症候性心不全患者において心血管死および心不全増悪イベントを有意に減少させること26)や、糖尿病とCKDを合併したHFpEFで心血管死を減少させること27)などが報告されています。SGLT2阻害薬と同様に、腎臓への作用や代謝の改善などを介して心不全の病態を改善する薬剤で、糖尿病・CKD合併例を中心に使用される機会が多いと考えられます。
HFmrEFはHFrEFに準じたアプローチを
HFmrEFについては、LVEF 40~49%のみを対象とした無作為化臨床試験が実施されていないため、明確なエビデンスをもつ治療薬はありません。ただし、HFmrEFはHFrEFに準じたアプローチをしても効果が認められるため、HFmrEFに対してはSGLT2阻害薬をベースに、病態に合わせてファンタスティック4を中心とした薬剤を併用することになります。
新規治療薬開発への期待
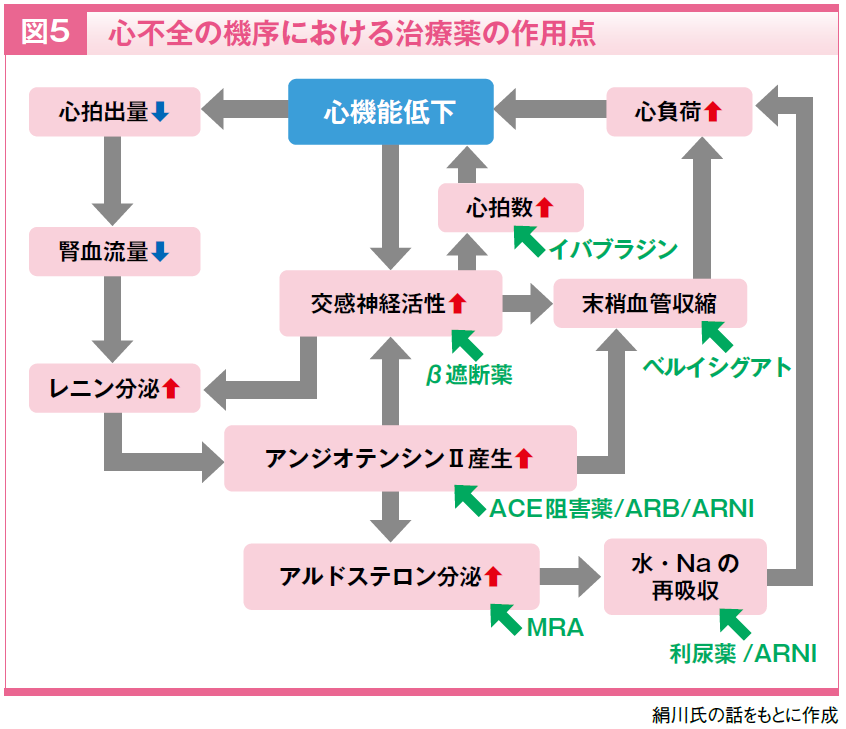
現在の治療薬の位置づけを心不全の機序の作用点ごとに表すと図5になります。なお、SGLT2阻害薬はまだ作用点がはっきりしていませんが、その登場はHFmrEF/HFpEF治療に大きな変化をもたらしました。
ただし依然として、その治療選択肢は限られています。HFmrEF/HFpEFにはさまざまな病態の患者が含まれていることから、それに合わせた個別化治療が必要であり、新たな治療薬の開発が待ち望まれています。
HFmrEF/HFpEF治療薬の候補として、現在、注目されているのがGLP-1受容体作動薬です。もともと糖尿病治療薬として開発された薬剤ですが、肥満を合併するHFpEF患者に対するGLP-1受容体作動薬がQOLの改善をもたらすこと28)やGIP/GLP-1共受容体作動薬が心血管死や心不全増悪イベントを減少することなどが報告されており29)、今後、特に肥満を伴うHFpEF患者に対して、こうした薬剤が治療の新たな選択肢として加わる可能性があります。ただし、これらのエビデンスの多くは欧米での研究成果であり、日本人肥満例における有効性や安全性については、今後の国内での検討結果が待たれます。
心不全マネジメントにおける薬剤師の役割
心不全の予後改善に向けては、悪化の兆候をいち早く捉え、迅速に介入することにより、重症化や再入院を防ぐことが不可欠です。薬剤師は、患者に最も近い医療従事者のひとりとして、患者に寄り添った実践的なアドバイスを提供する役割を担っています。
心不全マネジメントにおける課題の1つは、患者自身による治療の中断です。心不全治療により症状が改善すると、「もう大丈夫だ」と患者の自己判断で服薬を中止してしまうケースも少なくありません。そのため、薬剤師は心不全の標準治療を十分に理解したうえで、患者に対して服薬継続の意義を治療初期から繰り返し伝えていかなくてはなりません。
また、心不全悪化の徴候である体液貯留のヒントとなる体重変化の確認も欠かせません。患者に対しては「毎日体重を測定し、1〜2週間で2kg以上の変化があれば早めに受診を」と具体的な受診の目安を添えて説明してください。加えて、シックデイの対応についても、休薬のタイミングや受診の必要性など、状況に合わせた具体的な対応方法を事前に説明しておく必要もあります。
今回改訂されたガイドライン2)では、エビデンスに基づく薬物療法の推進はもちろんのこと、薬剤師を含むチームによる継続的な介入の重要性が強調されました。心不全という複雑な疾患に対して、薬剤師が専門性を活かして積極的に関わることは、患者のQOLや予後の向上に直結します。今回のガイドライン改訂が、より良い心不全マネジメントの実現に向けた一助となることを期待しています。
【参考文献】
1)Okura Y, et al. Circ J 2008; 72: 489-491.
2)日本循環器学会、日本心不全学会.2025 年改訂版 心不全診療ガイドライン.
https://www.j-circ.or.jp/cms/wp-content/uploads/2025/03/JCS2025_Kato.pdf
3)日本循環器学会、日本心不全学会.急性・慢性心不全診療ガイドライン(2017年改訂版).
4)日本循環器学会、日本心不全学会.2021年 JCS/JHFS ガイドライン フォーカスアップデート版 急性・慢性心不全診療.
5)McDonagh TA, et al. Eur Heart J 2021; 42: 3599-3726.
6)McDonagh TA, et al. Eur Heart J 2023; 44: 3627-3639.
7)Heidenreich PA, et al. Circulation 2022; 145: e895-e1032.
8)Bozkurt B, et al. Eur J Heart Fail 2021; 23: 352-380.
9)Tsuji K, et al. Eur J Heart Fail 2017; 19: 1258-1269.
10)Kalogeropoulos AP, et al. JAMA Cardiol 2016; 1: 510-518.
11)Savarese G, et al. JACC Heart Fail 2019; 7: 306-317.
12)Halliday BP, et al. Lancet 2019; 393: 61-73.
13)エンレスト錠 添付文書 2024年5月改訂(第8版)
14)Packer M, et al. N Engl J Med 1996; 334: 1349-1355.
15)CIBIS-II Investigators and Committees. Lancet 1999; 353: 9-13.
16)MERIT-HF Study Group. Lancet 1999; 353: 2001-2007.
17)McMurray JJV, et al. N Engl J Med 2019; 381: 1995-2008.
18)Packer M, et al. N Engl J Med 2020; 383: 1413-1424.
19)Ferreira JP, et al. J Am Coll Cardiol 2021; 77: 1397-1407.
20)Zelniker TA, et al. J Am Coll Cardiol 2020; 75: 422-434.
21)Butt JH, et al. Circulation 2022; 146: 1210-1224.
22)Butt JH, et al. Ann Intern Med 2022; 175: 820-830.
23)Adamson C, et al. Eur Heart J 2022; 43: 4406-4417.
24)Anker SD, et al. N Engl J Med 2021; 385: 1451-1461.
25)Solomon SD, et al. N Engl J Med 2022; 387: 1089-1098.
26)Solomon SD, et al. N Engl J Med 2024; 391: 1475-1485.
27)Vaduganathan M, et al. Nat Med 2024; 30: 3758-3764.
28)Kosiborod MN, et al. N Engl J Med 2023; 389: 1069-1084.
29)Packer M, et al. N Engl J Med 2025; 392: 427-437.
絹川 真太郎 氏
1994年九州大学医学部卒業、九州大学循環器内科入局、2000年医学博士取得、2001年ニューヨーク医科大学留学、2005年北海道大学病院医員、2007年北海道大学大学院医学研究科助教、2012年同講師、2020年九州大学大学院医学研究准教授。2025年より現職。心不全の分子機構の解明、運動能力低下および骨格筋異常の分子機序の解明などの研究に従事してきた。