監修
北里大学病院 精神神経科 主任教授
稲田 健 氏
うつ病の患者数は増加の一途を辿り、うつ病の薬物療法は専門医だけでなく非専門のクリニックでも実施されることがあります。うつ病の薬物療法では患者の自己判断による中断、細かい用量調整や薬剤の変更などの難しさが指摘されています。また、症状にかかわらず薬物療法が長期間続く患者や、再発を繰り返す患者もいることから、治療をいつまで継続すべきかが課題となります。うつ病の専門医の北里大学病院精神神経科主任教授 稲田健氏の解説で、うつ病の薬物療法を中心に治療開始から出口戦略のカギについて学習していきましょう。
うつ病の症状と診断基準
重症度評価と精神病性の特徴
まず、うつ病の定義ですが、抑うつ気分、興味・喜びの消失の少なくともどちらか一方と、さらに身体症状と精神症状を含めて5つ以上の症状が、2週間以上ほぼ毎日続いているとうつ病と診断されます(表1)。
また、うつ病の治療にあたっては、まず重症度を適切に評価することが大切です。
重症度は大まかに、軽症はうつ病の診断基準を満たすものの社会生活はなんとか維持される状態、中等症では社会的機能が著しく低下し休職・休学が必要な状態、重症は食事・入浴など基本的生活動作も困難となり時に入院治療を要する状態です。なお、重症度にかかわらず、うつ病は自傷・自殺の切迫性評価が重要となります。
また、重症度の評価とともにうつ病が精神病性の特徴を伴っているか否かの評価を行います。うつ病で見られる精神病性の特徴として「妄想」があげられます。精神医学でいう妄想とは、事実と異なることを強く確信し訂正できない思考を指します。うつ病に伴いやすい妄想としては、罪業妄想(自らの罪や過失を過大視し罰を受けると確信する)、貧困妄想(実際には経済的問題がないのに破産すると信じ込む)、心気妄想(治癒不能の疾患に罹患していると確信する)があります。
うつ病治療の基本は基礎的介入
重症度に応じた薬物療法、状況に応じて入院治療も
うつ病の治療としては、まず、治療の基本となる「基礎的介入」を実施します。基礎的介入とは、支持的精神療法や心理教育などを含む、患者さんに対する基本的なサポートです。相槌で共感を示す、感情をそのまま返す(感情の反射)など受容的に支援するほか、うつ病という疾患の性質や治療法、対処法などの情報を患者さんやご家族に提供することで、疾患についての理解を深め治療・再発予防を促進します。基礎的介入は、全てのうつ病治療のベースとなります。
その後、重症度に応じ、薬物療法と非薬物療法(認知行動療法など体系化された精神療法)の組み合わせを選択し開始していきます。軽症例の場合は基礎的介入だけでも治療は可能です。患者さんが希望するようであれば抗うつ薬を使用しますが、抗うつ薬が顕著に奏功するのは基本的に中等症以上ですので、軽症例では過剰治療にならないよう注意が必要です。中等症以上では、外来で対応可能か、入院が必要かを検討し、速やかに抗うつ薬単剤による薬物療法を開始します。精神病性の特徴を伴う場合は抗うつ薬に抗精神病薬を併用して治療を進めていきます。
抗うつ薬は単剤・低用量から治療開始
第2世代抗うつ薬が推奨される
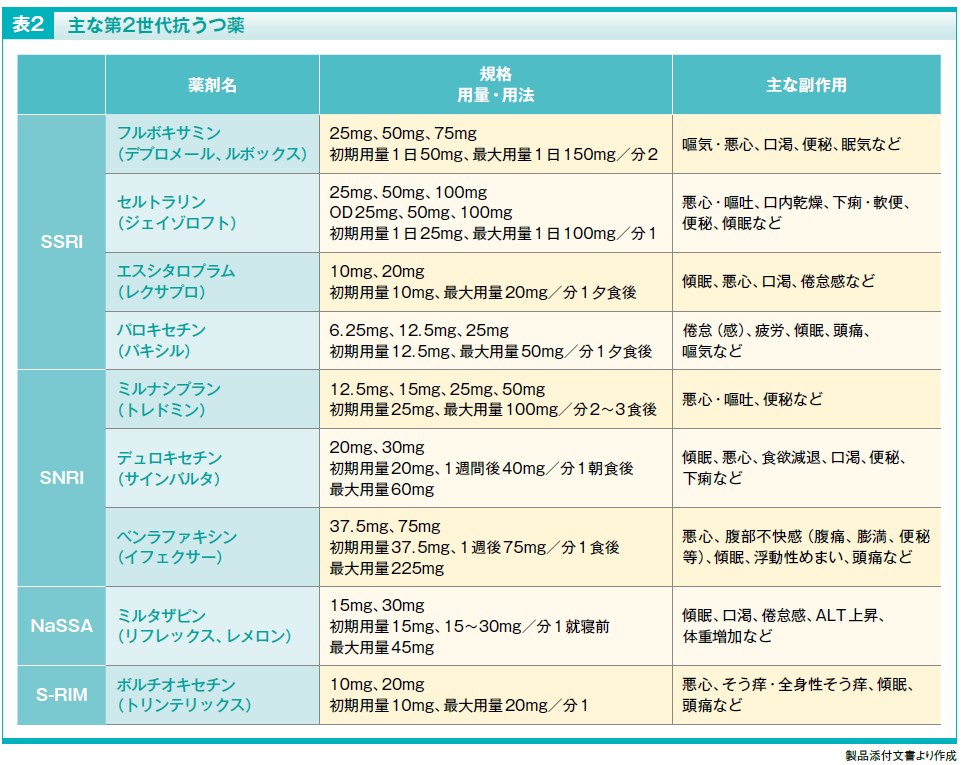
薬物療法は、まず、抗うつ薬の単剤・低用量として開始します。主に、選択的セロトニン再取り込み阻害薬(SSRI)、セロトニン・ノルアドレナリン再取り込み阻害薬(SNRI)、ノルアドレナリン作動性・特異的セロトニン作動性抗うつ薬(NaSSA)、セロトニン再取り込み阻害・セロトニン受容体調節薬(S-RIM)といったいわゆる第2世代の抗うつ薬を選択することが推奨されています(表2)。比較的古くから存在するタイプの三環系や四環系抗うつ薬は、副作用の種類や頻度の多さから現在では使用されづらくなっています。
第2世代抗うつ薬の中の薬剤選択については、いずれの薬剤も有効性の面では大きな差がないとされているため、特定の薬剤が第一選択などの推奨はありません。ただし、不眠や焦燥が強ければNaSSAのミルタザピンを選択、比較的軽症であれば眠気が少ないSSRIを選択するのが良い、といったエキスパートの見解もあります。
抗うつ薬初期は効果より副作用が先行
服用中断を抑止のために事前説明が肝要
抗うつ薬の服用開始時に非常に重要な点として私がお示ししたいのは、「患者が抗うつ薬の効果を体感するよりも先に副作用の発現がある、という点を患者に事前に十分説明しておくこと」です。
抗うつ薬の服用初期や増量時には、不安や焦燥感、攻撃性、衝動性、動悸などが高まるといったアクチベーション症候群(賦活症候群)が見られることがあります。一方で、抗うつ薬の効果が現れるまでには一定の期間(一般的に2 週間程度)を要します。初期の副作用について患者さんへの説明が不十分なまま治療を開始してしまうと、有効性が体感される前に副作用が発現することで、服用中断が起こりやすくなり治療継続自体が困難となってしまいます。
副作用が先行する場合があること、副作用が発現しても許容できるようであれば次回の診察までは服用を続けてもらうこと、副作用が辛くて服用できない場合には他の薬剤に切り替えることができることなどをあらかじめ説明しておくことは非常に重要な事項です(表3)。なお、服用後一定期間を過ぎて抗うつ薬の効果が出てきたとしても、副作用が継続するようであれば服用継続も難しくなりますので他剤への切り替えを検討します。
薬物療法の治療アルゴリズム
最大用量まで増量後に効果判定し、次の選択
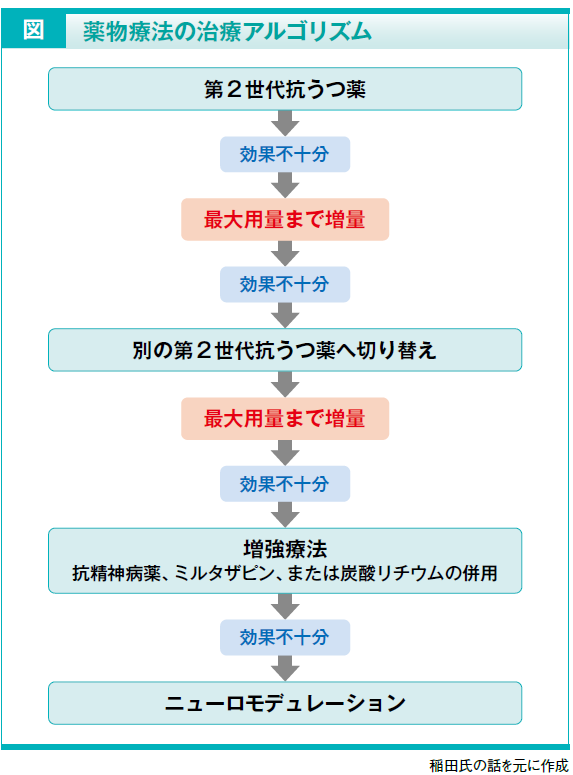
抗うつ薬を服用後、一定期間が過ぎても効果が不十分な場合には、副作用の発現状況を確認しながら最大用量まで増量していきます。
そして、最大用量で4~6 週間程度経過しても効果が不十分であれば、別の抗うつ薬に切り替えて再度、最大用量まで漸増していきます。それでも効果が不十分な場合には増強療法として抗精神病薬や、NaSSAのミルタザピン、気分安定薬の炭酸リチウム(保険適用外)の併用を検討します。それでも難しい場合は後述のニューロモデュレーションという手段を検討します(図)。
うつ病の増強療法として保険適用がある抗精神病薬は、アリピプラゾールとブレクスピプラゾールですが、オランザピン(保険適用外)やクエチアピン(保険適用外)も増強療法に多く用いられています。オランザピンやクエチアピンは鎮静効果が強いという特徴があるため、不安や焦燥感、不眠が強い症例には非常に有効です。また、以前は四環系抗うつ薬であるミアンセリンが、やはり鎮静効果が強いことから併用薬として用いられていましたが、今は抗うつ薬を併用する場合には、第2世代抗うつ薬の中で鎮静効果が強いミルタザピンの併用が行われることが多くなっています。
古くから増強療法に用いられてきた炭酸リチウムも効果は高いものの、治療濃度が中毒濃度と近接しているため、副作用の出現に注意が必要であり、定期的な血中濃度測定が必要となります。
ニューロモデュレーション治療
電気や磁気で脳の神経を刺激
増強治療を行っても改善が見られない場合には、次の手段として電気や磁気などによって脳の神経を刺激して働きを調整する「ニューロモデレーション治療」が行われることがあります。
ニューロモデュレーション治療には、「反復性経頭蓋磁気刺激療法(rTMS)」と「修正電気けいれん療法(mECT)」があります。mECTの効果は高く、重症で入院治療を行っても全く改善が見られず自殺企図が切迫しているような難治例に対しては、積極的に施行を試みるべき治療法とも言えます。ただし、mECTは全身麻酔が必要であるなど実施できる施設が限られ、rTMSは保険診療で行える医療施設もまだ多くありません。したがって、ニューロモデレーション治療は一般的とはいえない手段です。
抗不安薬の位置づけ
治療脱落率の低減に有効だが短期間の使用に
以前は、うつ病治療の初期段階からベンゾジアゼピン系抗不安薬を抗うつ薬と併用することがスタンダードとされていました。現在では、抗不安薬にはうつ病を改善させる作用は見られず対症療法という位置づけである点、依存や乱用の懸念がある点が指摘されています。こうしたことから、うつ病の治療には抗不安薬は可能な限り用いません。
ただし、ベンゾジアゼピン系抗不安薬は、特に不安や焦燥が強いケースで、治療初期の抗うつ薬の効果が発現するまでの期間に併用すると治療脱落率が低減できることも示されています。この場合も、漫然とそのまま使用を継続すると依存が形成され服用中止が困難になりますので、短期間の使用にとどめるべきと考えています。
抗不安薬を使用する際には、「この薬は症状が安定したらなるべく早くやめるべき薬です」という点を、やはり初期に患者さんにしっかりと説明しておくことが重要です。その上で私は「不安や焦燥が強くてどうしても耐えられないような時には飲んでもいいですよ」と伝えて頓服で処方して、いわば「お守り」のように保持してもらうようにしています。
また、ベンゾジアゼピン系以外の抗不安薬としてセロトニン1A受容体部分作動薬があります。この薬剤は、依存性がなく安全性が高いという利点はあるものの、効果が比較的強くはない、効果発現までに2週間近くかかる、といったネガティブ要素も持ち合わせています。うつ病の治療開始時の併用薬というよりも、依存性の問題などからベンゾジアゼピン系抗不安薬を用いることが困難な症例に用いるのに適した薬剤といえます。
うつ病は再発を繰り返すたびに再発率が上昇
再発予防のための抗うつ薬の継続期間は?
うつ病の急性期症状を脱した後の維持期は、主に再発予防を目的に治療していきます。ここでうつ病が再発してしまうと、その後はさらに再発しやすくなり、再発を繰り返すたびに再発リスクが上がる悪循環に陥りますので、経過を慎重に管理していく必要があります。
再発を防ぐために大切なのが基礎的介入です。日常生活のリズムを整えるや、症状が改善したからといって無理はしないなど、再発を起こさないための生活を患者さんにしっかり身につけてもらいます。
また、抗うつ薬による治療をどの程度継続するべきでしょうか。治療を継続した場合と中止した場合で6カ月間の再発率を検討したシステマティックレビューでは、継続した場合の再発率は約20%、中止した場合の再発率は約40%であり、継続による再発予防効果は1年6カ月程度までは変わらないことが示されています1)。こうした結果を踏まえ、寛解後少なくとも6カ月間は抗うつ薬を継続することが推奨されています。
その後の治療については、個々の患者さんが上記の20%または40%の再発率をどう捉えるかによります。例えば、再発は絶対にしたくない、あんな辛い思いはしたくないという患者さんであれば、20%と40%の差は大きいと捉えて服用継続を希望するかもしれませんし、重症度がそこまで高くなかった患者さんでは、薬を中止しても60%の人は再発しないのであれば、薬は中止したいと思うかもしれません。抗うつ薬の継続か中止かについては患者さんごとに話し合って決めていくことになります。
うつ病で残遺しやすい不眠と認知機能障害
残存不眠は再発リスクと関与
うつ病の症状に改善が見られて寛解に至ったとしても、全てが発症前の状態まで戻るとは限らず何らかの症状が残ることがあります。残遺しやすい症状として不眠や、記憶力や集中力の低下といった認知機能障害があります。
これらのうつ病の残遺症状は予後に悪影響をおよぼすことが指摘されています。われわれが行ったレセプトデータの解析から残存不眠と再発の関係を検討した研究では、残存不眠がない群に比べて残存不眠がある群では、再発までの期間が有意に短く(p<0.001、カイ二乗検定)、 1年再発率が高く(7.4% vs 43.4%)、再発リスクが有意に高いことが示されました(p<0.0001、カイ二乗検定)2)。つまり、残存不眠は重要な再発リスク因子であると考えられ、不眠が残遺している場合には、より再発に注意して生活を整えていくことがとても大切なのです。
うつ病治療の出口戦略
カギとなるのは不眠治療
うつ病において、「不眠」は特に重視すべき症状です。他の精神疾患で、診断基準に不眠が入っているものはほとんどありません。うつ病の場合、重要な症状として不眠が診断基準に入っていることからもその重要性がわかります。
実は、うつ病における不眠をどう捉えるかについては大きく2つの考え方があり、これによって睡眠薬の処方の是非が変わってきます。考え方の一つは「不眠はうつ病の症状である」、もう一つは「不眠はうつ病のトリガーになる」です。不眠はうつ病の症状とする前者であれば、うつ病の状態を良くすれば不眠もおのずと改善するということになります。つまり、その治療は鎮静効果が強いミルタザピンのような抗うつ薬を使えば良いということになり、睡眠薬は併用すべきではないという考え方に至ります。一方で、不眠はうつ病の独立したリスクとして捉える後者の考え方では、不眠は単独で治療をすべきだということになりますので、睡眠薬を積極的に使用するという考え方になります。
もちろん、うつ病診療を行う全ての医師がこのいずれかだけに立って治療しているわけではないと思います。目の前の患者さんが不眠で苦しんでいるのですから、睡眠薬を使って改善していこうとなるわけで、うつ病の患者さんの半数は睡眠薬を併用して治療が行われているのが実情です。しかしながら、前述の残存不眠の問題もあることから、うつ病における不眠は慎重に管理していくべき症状です。
不眠治療の基本は睡眠衛生指導
薬物療法の第一選択薬はオレキシン受容体拮抗薬
不眠に対する治療としては、まずは、適正な睡眠時間を確保し、休養感を高めるために生活習慣や睡眠環境等の見直しを睡眠衛生指導として実施することが非常に重要です。
その上で、睡眠薬を使用する場合にどの薬剤を選択するかについては、前述の通り、ベンゾジアゼピン系受容体作動薬のリスクや依存の問題から、現在はベンゾジアゼピン系受容体作動薬の使用は推奨されていません。いわゆるZドラッグといわれる非ベンゾジアゼピン系は、ベンゾジアゼピン系の薬剤に比べて安全性は高いといわれていますが、やはりある程度のリスクはあります。
現在、うつ病に対する睡眠薬としては、依存や離脱症状が少ないオレキシン受容体拮抗薬が第一選択薬となります。メラトニン受容体作動薬についてはうつ病患者では効果が強く見られないことから、睡眠覚醒リズムを整えるための補助や、高齢者で副作用が非常に問題になる場合に選択するなど限定的に使用されていると思います。
第一選択となるオレキシン受容体拮抗薬は、現在の3剤に加え、ボルノレキサントの製造販売が承認されました(2025年8月)(表4)。これらの薬剤の中でどれを選択するかについて、ダリドレキサントは発売後まだそれほど期間が経っていないのでデータや治療経験が少ないのですが、スボレキサントとレンボレキサントでは、レンボレキサントで若干効果が高く、特に入眠困難に効果が高い印象があります。スボレキサントは入眠困難には少し効果が弱いのですが、中途覚醒には効果が高いとされています。また、レンボレキサントは薬物相互作用が少なく一包化も可能であるなど、効果面だけではなく、用量調節のしやすさなど使いやすさも加味して選択します。
オレキシン受容体拮抗薬の副作用
「悪夢」はなぜ起こるのか
オレキシン受容体拮抗薬で問題となる副作用が「悪夢」です。
オレキシンは覚醒と睡眠を調節する神経伝達物質で、受容体に作用することで覚醒システムを活性化します。この覚醒維持システムが過剰に働くことで不眠が引き起こされることから、オレキシンの作用を阻害することで覚醒システムを抑制し睡眠状態へ移行させるのがオレキシン受容体拮抗薬の作用機序です。
オレキシン受容体拮抗薬で悪夢をみる原因ははっきりとはわかっていません。人間はレム睡眠とノンレム睡眠のどちらでも夢を見ているのですが、記憶に残りやすいのが眠りの浅いレム睡眠中の夢といわれています。オレキシンは受容体に結合することでレム睡眠を抑制しているため、オレキシン受容体拮抗薬でその作用を阻害するとレム睡眠が増加し、夢をみるという現象が増加します。自然な睡眠と覚醒の切り替わりとは異なり、オレキシン受容体拮抗薬による睡眠では、レム睡眠と覚醒が突如切り替わる、健忘作用がないため夢の記憶が増える、といった特徴があるとされています。
しかし、なぜ悪夢なのか。人間は夢を見たとしても起床時には忘れてしまうことが多いのですが、いろいろな情動や深い感情と結びついたような夢は記憶として残りやすいことから悪夢だけが記憶に残りやすいのではないか、というのが睡眠の専門家の見解です。実際に、心理的なストレスがなくなると悪夢も見なくなるというケースを臨床で多く経験します。
ここでも大切なのは、悪夢を見ることがあるとしてもそれはオレキシン受容体拮抗薬の服用による作用の可能性が高いと事前に患者さんに説明しておくことです。この説明がないままオレキシン受容体拮抗薬を服用すると、患者さんは悪夢への恐怖から服用中断が起きかねません。いつまでも不眠の症状が改善されないだけでなく、うつ病も改善されないという悪循環につながってしまいます。
多角的な心理的アプローチで患者さんをサポート
治療を通じて生活や考え方を整える手助けを
今回は薬物療法にフォーカスして解説してきましたが、うつ病の治療は薬物療法だけで完結するわけではありません。薬物療法と並行して、うつ病発症の原因となった生活を見直して、無理のない生き方をしていけるように 手助けする心理的アプローチが非常に重要です。それらの治療を通じて生活や考え方を整えていくことは人間的な成長にもつながりますので、私はうつ病発症前よりもその人の人格の水準は上がると思っていますし、うつ病治療はそこを目指していいのではないかと思っています。
また、うつ病の薬物療法では、治療継続という面から 患者さんへの説明が重要な場面が多くあります。薬剤師の皆さんには一般的な服薬指導というだけでなく、薬物療法の副作用や有害事象などのデメリットを最小化して、効果を最大化にするには心理的な関わりが重要となることを理解して、その患者さんが今生活の中で何に困っているのかを知り、共感してサポートするような支持的介入してもらえたらと思っています。
【参考文献】
1)Kato M, et al. Discontinuation of antidepressants after remission with antidepressant medication in major depressive disorder: a systematic review and meta-analysis. Mol Psychiatry. 2021; 26: 118-33.
2)Ken Inada, et al. Effect of residual insomnia and use of hypnotics on relapse of depression: a retrospective cohort study using a health insurance claims database. J Affect Disord. 2021; 281: 539-546.
稲田 健 氏
1997年北里大学医学部卒業、北里大学医学部精神科入局。北里大学大学院医療系研究科博士課程修了。アメリカ合衆国ノースカロライナ大学留学。東京女子医科大学医学部精神医学講座助教、講師、准教授を経て、2022年より現職。精神保健指定医。日本精神神経学会専門医・指導医。日本臨床精神神経薬理学会専門医。